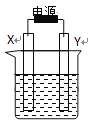
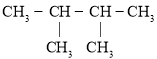��Ŀ����
����Ŀ��X��Y��Z��WΪ���ֳ����Ķ�����Ԫ�ء�����YԪ��ԭ�Ӻ�������������������Ӳ�����3�������������ڱ��е����λ����ͼ��ʾ��
X | Y | |
Z | W |
��ش��������⣺
��1��W�����ڱ���λ��_____��
��2��X�����ܹ�����+1�������ӣ������ʽ��_____��Y����̬�⻯���Z����̬�⻯��ķе�ߣ�Ե����_____��
��3��X������������ˮ���������⻯���ܻ�������M��M��ˮ��Һ�����Ե�Ե����_____(�����ӷ���ʽ��ʾ)��
��4����Y��Z�����һ����̬������Q��Q����W�ĵ����ڳ�ʪ�����з�Ӧ����Ӧ�Ļ�ѧ����ʽ��_____��
����һ�������£�������Q��Y�ĵ��ʷ�Ӧ��ƽ��ʱ��������̬���ʣ���Ӧʱ��ÿת��4mol���ӷ���190.0kJ���÷�Ӧ���Ȼ�ѧ����ʽ��_____��
���𰸡���������VIIA��  ˮ���Ӽ������� NH4++H2O=
ˮ���Ӽ������� NH4++H2O=![]() +H+ SO2+Cl2+2H2O=H2SO4+2HCl 2SO2��g��+O2��g��=2SO3��g��
+H+ SO2+Cl2+2H2O=H2SO4+2HCl 2SO2��g��+O2��g��=2SO3��g��![]() =-190.0kJ
=-190.0kJ![]() mol-1
mol-1
��������
YԪ��ԭ�Ӻ�������������������Ӳ�����3����˵�����������Ӳ㣬����������Ϊ6����YΪ��Ԫ�أ�����Ԫ�����ڱ������λ�ÿ���֪XΪ��Ԫ�ء�ZΪ��Ԫ�ء�WΪ��Ԫ�ء�
��1���ɷ�����֪WΪ��Ԫ�أ������ڱ��ĵ�������VIIA�壬�ʴ�Ϊ����������VIIA�壻
��2��XΪ��Ԫ�أ������ܹ�����+1��������Ϊ笠��������ʽ�� ��Y����̬�⻯����ˮ��Z����̬�⻯�������⣬��Ϊˮ���Ӽ��ܹ��γ����������ˮ�ķе������ķе�ߣ��ʴ�Ϊ��
��Y����̬�⻯����ˮ��Z����̬�⻯�������⣬��Ϊˮ���Ӽ��ܹ��γ����������ˮ�ķе������ķе�ߣ��ʴ�Ϊ�� ��ˮ���Ӽ���������
��ˮ���Ӽ���������
��3��X������������ˮ���������ᣬ���⻯���ǰ����������ܻ�������M������泥�����淋�ˮ��Һ����Ϊ笠�����ˮ��������ԣ���ˮ������ӷ���ʽΪNH4++H2O=![]() +H+���ʴ�Ϊ��NH4++H2O=
+H+���ʴ�Ϊ��NH4++H2O=![]() +H+��
+H+��
��4����QΪ��������W�ĵ���Ϊ�����������ڳ�ʪ�Ļ������ܷ���������ԭ��Ӧ���䷴Ӧ�ķ���ʽΪSO2+Cl2+2H2O=H2SO4+2HCl���ʴ�Ϊ��SO2+Cl2+2H2O=H2SO4+2HCl��
�ڻ�����QΪ��������Y�ĵ���Ϊ���������߷�Ӧ��������������2mol��������Ӧת��4mol���ӣ����ų�190.0kJ����������Ӧ���Ȼ�ѧ��Ӧ����ʽΪ2SO2��g��+O2��g��=2SO3��g��![]() =-190.0kJ
=-190.0kJ![]() mol-1���ʴ�Ϊ��2SO2��g��+O2��g��=2SO3��g��
mol-1���ʴ�Ϊ��2SO2��g��+O2��g��=2SO3��g��![]() =-190.0kJ
=-190.0kJ![]() mol-1��
mol-1��

����Ŀ��ijͬѧͨ��ʵ���о�Na2O2��ˮ�ķ�Ӧ��
���� | ���� |
��ʢ������Na2O2���Թ��м�������ˮ���õ���Һa | ��Ӧ���ң�������ʹ������ľ����ȼ������ |
Ȼ������Һa�е������η�̪ | ��Һ�ȱ�죬����dz��Լ10������Һ��Ϊ��ɫ |
Ϊ��̽����Һ��Ϊ��ɫ��ԭ��ͬѧ���տ�ѧ�ij�����������ʵ�飺
����������裩
Na2O2��H2O��Ӧ�Ļ�ѧ����ʽ_____������Һa�еμӷ�̪��Ӧֻ���죬��ʵ���з��ַ�̪��������ɫ���ɴ�������µļ��裺
����A��O2��Ư���� ����B��NaOH��Ư���� ����C��O2��NaOH��ͬ������Ư����
��ʵ����۲죩
��2��������±���
ʵ���� | 1 | 2 | 3 |
ʵ��װ�� |
|
|
|
ʵ����� ���A������B����C���� | ����_____ | ����____ | ����__ |
ʵ������ | ��Һ����10���Ӿ��ޱ仯 | ||
ʵ����� | _____ | ||
���������ϣ�
��ͬѧ�������ϣ�H2O2��һ���ڼ��������²��ȶ�������Ư���Ե����ʡ�
����������裩
��ͬѧ��Ϊ��ɫ��ԭ���������Һa�д���H2O2��H2O2Ư���˷�̪��
��ʵ����۲죩
��3��ͨ��ʵ��֤ʵ��H2O2�Ĵ��ڣ�ȡ������Һa�������ɫ��ĩ____���ѧʽ�������ٲ�������ʹ������ľ����ȼ�����塣��ͬѧ��һ��ͨ��ʵ��֤ʵ����Һa�е����̪��H2O2���̪�����˻�ѧ��Ӧ��ʵ�鷽����ȡ������Һa���Թ��У�_____��
����������ۣ�
��4
����Ŀ����SO2�����̿�(��Ҫ�ɷ�ΪMnO2������Fe��Al��Ca��Pb�Ļ������)����ˮ����������Ϊԭ�Ͽ��Ʊ�MnSO4Һ��Mn3O4����Ҫʵ�鲽������
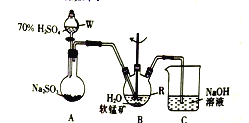
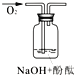
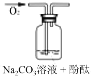
����I����ͼ��ʾװ�ã���SO2ͨ��B�е����̿�Һ��(MnO2+SO2=MnSO4)��
����II����ַ�Ӧ���ڲ��Ͻ���������������R�м�������������MnO2��MnCO3������������Na2S��Ǧ��
����III�����˵�MnSO4��Һ
(1)����R��������_______��
(2)װ��A������ȡSO2����Ӧ�Ļ�ѧ����ʽΪ_________��
(3)װ��B�еķ�ӦӦ������90~100�������˵ļ��ȷ�ʽ��______________��
(4)װ��C��������______________________��
(5)���������м��봿��MnO2��Ŀ����_______________����MnCO3������ҺpHʱ���������ҺpH�ķ�ΧΪ________(��ʵ�������£����ֽ������ӿ�ʼ�����ͳ�����ȫ��pH���±�)
�������� | Fe2+ | Fe3+ | Al3+ | Mn2+ |
��ʼ������pH | 7.04 | 1.87 | 3.32 | 7.56 |
������ȫ��pH | 9.18 | 3.27 | 4.9 | 10.2 |
(6)��֪���ÿ�������Mn(OH)2��Һ���Ʊ�Mn3O4[6Mn(OH)2+O2![]() 2Mn3O4+6H2O]����Ҫ������ΪMnOOH����Ӧ�¶Ⱥ���ҺpH�Բ�Ʒ��Mn������������Ӱ��ֱ���ͼ��ʾ
2Mn3O4+6H2O]����Ҫ������ΪMnOOH����Ӧ�¶Ⱥ���ҺpH�Բ�Ʒ��Mn������������Ӱ��ֱ���ͼ��ʾ

�ڷ�Ӧ�¶ȳ���80��ʱ��Mn3O4�IJ��ʿ�ʼ���ͣ�Mn(OH)2�ǰ�ɫ������Mn3O4�ʺ�ɫ��Mn3O4��MnOOH���̵�������������ֵ����Ϊ72.05����62.5%�벹�������ɲ���III�õ�MnSO4��Һ�����ð�ˮ���Ʊ��ϴ�����Mn3O4��ʵ�鷽����______________________����ո���6Сʱ�ò�ƷMn3O4��