题目内容
将2mol H2和1mol CO2充入体积为10L的恒容密闭容器中,在一定条件下发生反应:
①CO2(g)+ H2(g) CO(g) + H2O(g) △H1=+41.2kJ·moL-1;
CO(g) + H2O(g) △H1=+41.2kJ·moL-1;
②CO2(g)+ 3H2(g) CH3OH(g) + H2O(g) △H2=-49kJ·moL-1。
CH3OH(g) + H2O(g) △H2=-49kJ·moL-1。
反应100min后达到平衡,测得下表数据:
| 温度 | 转化率(%) | 物质的量(mol) | ||
| H2 | CO2 | CH3OH | CO | |
| 240℃ | | 10 | 0.05 | 0.05 |
下列说法正确的是
A.升高温度,反应①的平衡常数减小
B.升高温度,CH3OH的含量提高
C.H2转化率为10%
D.100min内,反应②的速率为v(CO2)=0.0001 mol·L-1·min-1
C
解析试题分析:A、反应①为吸热反应,所以升高温度,反应①的平衡常数增大,错误;B、反应②为放热反应,升高温度,反应②平衡向左移动,CH3OH的含量减少,错误;C、CO2(g)+ H2(g) CO(g) + H2O(g),反应①转化的H2为:n(H2)=n(CO)=0.05mol;CO2(g)+ 3H2(g)
CO(g) + H2O(g),反应①转化的H2为:n(H2)=n(CO)=0.05mol;CO2(g)+ 3H2(g) CH3OH(g) + H2O(g),反应②转化的H2为:n(H2)=3n(CH3OH)=3×0.05mol=0.15mol,所以H2转化率为:(0.05mol+0.15mol)÷2mol×100%=10%,正确;D、100min内,反应②的速率为v(CO2)=v(CH3OH)=" 0.05mol÷10L÷10min=0.0005" mol·L-1·min-1,错误。
CH3OH(g) + H2O(g),反应②转化的H2为:n(H2)=3n(CH3OH)=3×0.05mol=0.15mol,所以H2转化率为:(0.05mol+0.15mol)÷2mol×100%=10%,正确;D、100min内,反应②的速率为v(CO2)=v(CH3OH)=" 0.05mol÷10L÷10min=0.0005" mol·L-1·min-1,错误。
考点:本题考查化学反应速率、转化率和化学平衡的计算。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案在密闭容器中存在如下反应:A (g)+3B(g) 2C(g);△H<0,某研究小组研究了只改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:

下列判断一定错误的是
| A.图Ⅰ研究的是压强对反应的影响,且乙的压强较高 |
| B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高 |
| C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高 |
| D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用催化剂的效率较高 |
对可逆反应4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
| A.达到化学平衡时,4v正(O2)=5v逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| C.达到化学平衡时,若增加容器体积,则正反应速率增大,逆反应速率减小,平衡正向移动 |
| D.化学反应速率关系是:2v正(NH3)= 3v正(H2O) |
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1的NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55 ℃间溶液变蓝时间,55 ℃时未观察到溶液变蓝,实验结果如下图。据图分析,下列判断不正确的是( )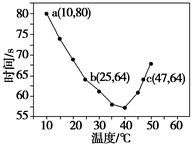
| A.40 ℃之前与40 ℃之后溶液变蓝的时间随温度的变化趋势相反 |
| B.图中b、c两点对应的NaHSO3反应速率相等 |
| C.图中a点对应的NaHSO3反应速率为5.0×10-5 mol·L-1·s-1 |
| D.温度高于40 ℃时,淀粉不宜用作该实验的指示剂 |
氢气既是最理想的能源又是重要的化工原料,用甲烷制氢气是一种廉价的制氢方法。有关的热化学方程式如下:
①CH4(g)+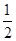 O2(g)
O2(g) CO(g)+2H2(g) ΔH<0
CO(g)+2H2(g) ΔH<0
②CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0
CO(g)+3H2(g) ΔH>0
下列说法不正确的是( )
| A.当反应①中v(CH4)正=v(CO)逆时,表明该反应达平衡状态 |
| B.其他条件不变时,增大体系压强,反应①、②中甲烷的转化率均减小 |
| C.使用高效催化剂可以加快反应速率,同时提高CH4的转化率 |
| D.同一容器内同时发生反应①与②时,容器内温度可能保持不变 |
对于可逆反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是 ( )。
4NO(g)+6H2O(g),下列叙述正确的是 ( )。
| A.反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(NH3)∶n(O2)=4∶5 |
| B.反应达到平衡时,对体系充入稀有气体并加压,平衡总是向逆反应方向移动 |
| C.反应达到平衡时,若向压强固定的密闭容器中充入稀有气体,平衡不移动 |
| D.当v正(NH3)∶v正(NO)=1∶1时,说明该化学反应已经达到平衡 |
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g) ΔH>0;该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )。
MgO(s)+CO2(g)+SO2(g) ΔH>0;该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )。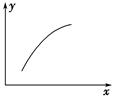
| 选项 | x | y |
| A | 温度 | 容器内混合气体的密度 |
| B | CO的物质的量 | CO2与CO的物质的量之比 |
| C | SO2的浓度 | 平衡常数K |
| D | MgSO4的质量(忽略体积) | CO的转化率 |
 2SO3(g) ΔH<0。经过相同的反应时间后,分别测定五个容器中SO2的转化率(α),并作出其随反应温度(T)变化的关系图。下列示意图中,不可能与实验结果相符的是( )
2SO3(g) ΔH<0。经过相同的反应时间后,分别测定五个容器中SO2的转化率(α),并作出其随反应温度(T)变化的关系图。下列示意图中,不可能与实验结果相符的是( )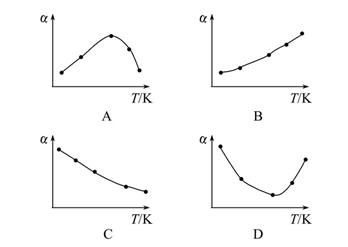
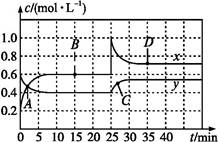
 N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是( )
N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是( )