题目内容
氨气是一种重要的化工原料,主要用于生产氮肥、硝酸、纯碱等化工产品。下图是合成氨,并联合生产硝酸、纯碱的简要流程示意图:
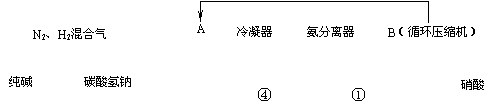 |
(1)设备A的名称是 ,设置循环B→A的目的是 。
(2)反应①的化学方程式是 。
反应③中氧化剂和还原剂的质量比为 。
(3)用两个化学方程式表示过程⑤中的反应过程。
(4)上述纯碱生产中过程⑤CO2的主要来源是 。
(1)合成塔 提高原料的利用率(或充分利用原料)
(2)1:2 4NH3+5O2=4NO+6H2O
(3)NH3+CO2+H2O=NH4HCO3 NaCl+ NH4HCO3 =Na HCO3↓+NH4Cl
(4)天然气等燃料与水的反应
(方程式2分,其余各1分)

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
氨气是一种重要的化工原料.下列关于氨气性质的描述不正确的是( )
| A、无色 | B、无味 | C、易液化 | D、极易溶于水 |
氨气是一种重要的化工产品,是生产铵盐、尿素等的原料.工业合成氨的反应如下:
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1.
(1)实验室中常用来制备氨气的化学方程式为 .
(2)已知H2(g)的燃烧热为285.8kJ?mol-1,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式 .
(3)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将 (填“正向”、“不”或“逆向”)移动,所滴加稀氨水的物质的量浓度为 mol?L-1.(25℃时,NH3?H2O的电离平衡常数Kb≈2×10-5).
(4)工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2].
CO2(g)+2NH3(g)
CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10mol CO2和0.40mol NH3,70min开始达到平衡.反应中CO2(g)的物质的量随时间变化如下表所示:
①20min时v正(CO2) 80min时v逆(H2O)(填“>”、“=”或“<”).
②在100min时,保持其它条件不变,再向容器中充入0.050mol CO2和0.20mol NH3,重新建立平衡后CO2的转化率与原平衡相比将 (填“增大”、“不变”或“减小”).
③根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变,则(t+10)℃下正确的图象可能是 (填图甲中的“A”或“B”).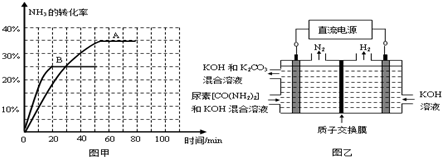
④图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素[CO(NH2)2]的碱性溶液制取氢气.该装置中阳极的电极反应式为 ,若两极共收集到气体22.4L(标况),则消耗的尿素为 g(忽略气体的溶解).
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1.
(1)实验室中常用来制备氨气的化学方程式为
(2)已知H2(g)的燃烧热为285.8kJ?mol-1,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式
(3)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将
(4)工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2].
CO2(g)+2NH3(g)
| 一定条件 |
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
②在100min时,保持其它条件不变,再向容器中充入0.050mol CO2和0.20mol NH3,重新建立平衡后CO2的转化率与原平衡相比将
③根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变,则(t+10)℃下正确的图象可能是

④图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素[CO(NH2)2]的碱性溶液制取氢气.该装置中阳极的电极反应式为
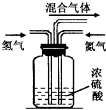 氨气是一种重要的化工原料,但随着工业化进程的加快,氨气也逐渐变成居室里一种重要的污染性气体.
氨气是一种重要的化工原料,但随着工业化进程的加快,氨气也逐渐变成居室里一种重要的污染性气体.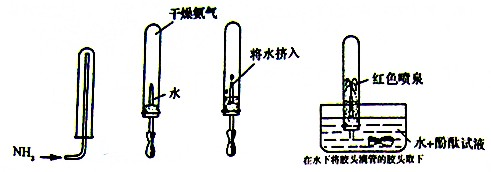
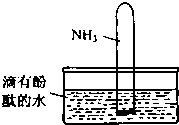 氨气是一种重要的化工原料.完成下列填空:
氨气是一种重要的化工原料.完成下列填空: