题目内容
【题目】在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为1.18g·cm-3。试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是________、________。
(2)取出这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是________。
(3)在40.0 mL 0.065 mol·L-1 Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过________mL。
(4)将不纯的NaOH样品1 g(样品含少量Na2CO3和水),放入50 mL 2 mol·L-1的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL 1 mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到________克固体。
【答案】
(1)36.5%;11.8 mol/L
(2)1 mol·L-1
(3)2.6
(4)5.85
【解析】
试题分析:(1)n(HCl)=![]() =10mol,m(HCl)=10mol×36.5gmol-1=365g,盐酸的质量分数w=
=10mol,m(HCl)=10mol×36.5gmol-1=365g,盐酸的质量分数w=![]() ×100%=36.5%,c(HCl)=
×100%=36.5%,c(HCl)=![]() =
=![]() mol/L=11.8mol/L,故答案为:36.5%、11.8mol/L;
mol/L=11.8mol/L,故答案为:36.5%、11.8mol/L;
(2)根据c(浓)V(浓)=c(稀)V(稀),可知:c(稀)=11.8molL-1×0.1L÷1.18L=1molL-1,故答案为:1molL-1;
(3)n(Na2CO3)=0.040L×0.065molL-1=0.0026 mol,
设加入稀盐酸的体积最多不超过xmL,则n(HCl)=1molL-1×0.001xL=0.001xmol,根据反应Na2CO3+HCl═NaHCO3+NaCl,可得0.0026=0.001x,解得x=2.6,故答案为:2.6;
(4)经过反应,蒸发中和后的溶液,最后所得固体为NaCl,根据Cl元素守恒:n(NaCl)=n(HCl)=0.050L×2molL-1=0.1mol,故m(NaCl)=0.1mol×58.5gmol-1=5.85g,故答案为:5.85g。

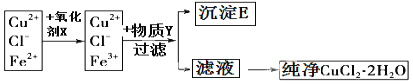
【题目】在氯化铜晶体(CuCl22H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其溶于水后加少量盐酸配制成水溶液,然后按如图所示的操作步骤进行提纯.
已知室温下,下列各物质的KSP:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp(25 ℃) | 8.0×10-16 | 2×10-20 | 4.0×10-38 |
(1)下列物质都可以作为氧化剂,其中最适合本实验的是 。
A.H2O2 B.KMnO4 C.HNO3 D.K2Cr2O7
写出你所选用的氧化剂在该实验中的发生反应的离子方程式: 。
(2)物质Y是 ,沉淀E的化学式 。
(3)从滤液得到纯净的CuCl22H2O晶体应采用的方法是 ,过滤、洗涤。
(4)假设加入Y之后Cu2+的浓度为0.02 mol/L,要使 Cu2+不水解,则加入Y后溶液的pH不能超过 。