题目内容
【题目】A、B、C三种不同的物质中均含有同一种元素,它们之间存在如图所示的转化关系(部分反应物及生成物已略去)。请回答下列问题:
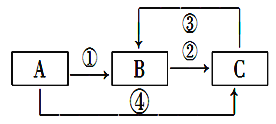
(1)若常温时B为红棕色气体,C为无色气体,则B生成C的化学方程式:____________。
(2)若常温时A为气态氢化物,B为淡黄色固体,C为气体,则CO2中混有少量气体C杂质可以用_________________来除(写一种即可)。
(3)若A为金属氧化物,B为工业制玻璃的主要原料之一,常温时0.1mol/L的C溶液的pH值为13,则检验A、B、C中共有的金属离子的方法是_____________________;现象为____________________。
(4)若常温时A为气体单质,①②③④均为化合反应,C的相对分子质量大于B,则C的电子式为:_____________________。
(5)若A是第三周期某金属的氧化物,B、C均为正盐且B的水溶液呈酸性,C的水溶液呈碱性。请写出反应③的离子方程式:________________________________________。
(6)若反应②③④均为化合反应,反应①为置换反应。当A为一种金属单质时,B中阳离子的检验方法为_________________________________________(写出具体操作过程)。
【答案】 3NO2 + H2O = 2HNO3 + NO 饱和NaHCO3溶液或酸性KMnO4溶液等合理答案均可 焰色反应 焰色为黄色 ![]() AlO2- + 4H+ = Al3+ + 2H2O 取少量B溶液于试管中,滴加少量KSCN溶液,无明显现象,再滴加少量新制氯水,若出现血红色则B中含Fe2+离子(用氢氧化钠沉淀法或K3[Fe(CN)6]沉淀法等合理均可,用酸性高锰酸钾不可)
AlO2- + 4H+ = Al3+ + 2H2O 取少量B溶液于试管中,滴加少量KSCN溶液,无明显现象,再滴加少量新制氯水,若出现血红色则B中含Fe2+离子(用氢氧化钠沉淀法或K3[Fe(CN)6]沉淀法等合理均可,用酸性高锰酸钾不可)
【解析】(1). 常温时B为红棕色气体,C为无色气体,说明B为NO2,C为NO,A为HNO3,B生成C的化学方程式是:3NO2 + H2O = 2HNO3 + NO,故答案为:3NO2 + H2O = 2HNO3 + NO;
(2). 常温时A为气态氢化物,B为淡黄色固体,说明B为S,A为H2S,C为SO2,则CO2中混有少量气体SO2杂质时,可以选用饱和的NaHCO3溶液或酸性KMnO4溶液除去SO2,故答案为:饱和NaHCO3溶液或酸性KMnO4溶液等;
(3). 常温时0.1mol/LC溶液的pH值为13,则C溶液中c(OH-)= 0.1mol/L,说明C是一元强碱,结合B为工业制玻璃的主要原料之一,说明B是碳酸钠,C为氢氧化钠,A为氧化钠或过氧化钠,则三种物质中含有的相同金属元素是钠元素,检验钠元素常用焰色反应,现象是焰色为黄色,故答案是:焰色反应;焰色为黄色;
(4).若常温时A为气体单质,①②③④均为化合反应,C的相对分子质量大于B,符合题意的是A为氧气,B为CO,C为CO2,①②③④对应的化学反应方程式分别为:2C+O2![]() 2CO、2CO+O2
2CO、2CO+O2![]() 2CO2、CO2+C
2CO2、CO2+C![]() 2CO、C+O2
2CO、C+O2![]() CO2,故C的电子式为:
CO2,故C的电子式为:![]() ,故答案为:
,故答案为:![]() ;
;
(5).若A是第三周期某金属的氧化物,B、C均为正盐且B的水溶液呈酸性,C的水溶液呈碱性,说明该金属是铝,A为氧化铝,B溶液含有铝离子、C溶液含有偏铝酸根离子,偏铝酸根离子反应生成铝离子的反应方程式是:AlO2- + 4H+ = Al3+ + 2H2O,故答案为:AlO2- + 4H+ = Al3+ + 2H2O;
(6).若反应②③④均为化合反应,反应①为置换反应。当A为一种金属单质时,说明A为单质铁,B为Fe2+、C为Fe3+,①②③④对应的反应方程式可以是:Fe+2HCl=FeCl2+H2↑、2FeCl2+Cl2=2FeCl3、2FeCl3+Fe=3FeCl2、2Fe+3Cl2![]() 2FeCl3,则检验Fe2+的实验方法是:取少量B溶液于试管中,滴加少量KSCN溶液,无明显现象,再滴加少量新制氯水,若出现血红色则B中含Fe2+离子,也可以用氢氧化钠沉淀法或K3[Fe(CN)6
2FeCl3,则检验Fe2+的实验方法是:取少量B溶液于试管中,滴加少量KSCN溶液,无明显现象,再滴加少量新制氯水,若出现血红色则B中含Fe2+离子,也可以用氢氧化钠沉淀法或K3[Fe(CN)6