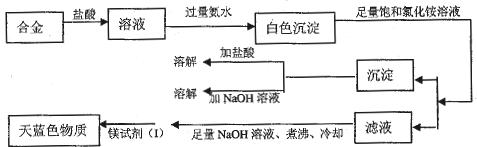
题目内容
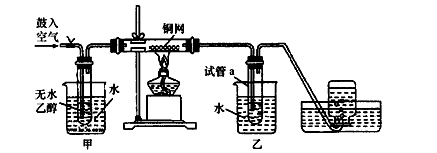
某化学课外小组用如图所示装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
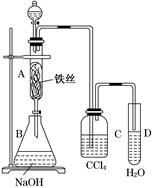
(1)写出A中反应的化学方程式________________。
(2)观察到A中的现象是____________________________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________________,写出有关的化学方程式___________________。
(4)C中盛放CCl4的作用是____________________。
(5)若证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入__ _,现象是_______________________ 。

(1)写出A中反应的化学方程式________________。
(2)观察到A中的现象是____________________________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________________,写出有关的化学方程式___________________。
(4)C中盛放CCl4的作用是____________________。
(5)若证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入__ _,现象是_______________________ 。
(10分)(1) 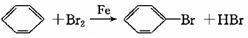
(2)反应液微沸,有红棕色气体充满A容器 (3)除去溶于溴苯中的溴
Br2+2NaOH=NaBr+NaBrO+H2O 或 3Br2+6NaOH=5NaBr+NaBrO3+3H2O
(4)除去溴化氢气体中的溴蒸气 (5)石蕊试液 溶液变红色(其他合理答案都对)

(2)反应液微沸,有红棕色气体充满A容器 (3)除去溶于溴苯中的溴
Br2+2NaOH=NaBr+NaBrO+H2O 或 3Br2+6NaOH=5NaBr+NaBrO3+3H2O
(4)除去溴化氢气体中的溴蒸气 (5)石蕊试液 溶液变红色(其他合理答案都对)
试题分析:(1)装置A中用来制备溴苯的,所以A中反应的化学方程式是
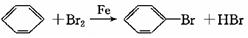 。
。(2)由于该反应是放热反应,且单质溴易挥发,所以实验中观察到的实验现象是反应液微沸,有红棕色气体充满A容器。
(3)由于生成的溴苯中含有溶解的单质溴,所以让反应液流入氢氧化钠溶液中的目的是除去溶于溴苯中的溴,有关反应的方程式是Br2+2NaOH=NaBr+NaBrO+H2O,或3Br2+6NaOH=5NaBr+NaBrO3+3H2O。
(4)由于单质溴易挥发,会干扰溴化氢的检验,所以四氯化碳的作用是除去溴化氢气体中的溴蒸气。(5)由于溴化氢溶于水溶液显酸性,据此可以检验,即向试管D中加入石蕊试液,而实验现象是溶液变红色。
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,针对性强,主要是考查学生对溴苯制备原理、物质的除杂、物质的检验的了解掌握情况,有助于培养学生规范严谨的实验设计能力,有利于提高学生的应试能力,有助于提升学生的学科素养。

练习册系列答案
相关题目
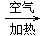 CuO
CuO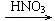 Cu(NO3)2
Cu(NO3)2 CuSO4
CuSO4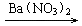 Cu(NO3)2
Cu(NO3)2