题目内容
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
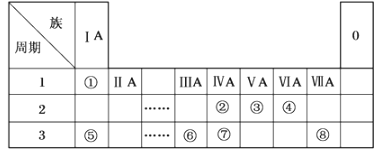
(1)①、②、③、④分别是_____、______、______、_____(用元素符号表示)
(2)描述⑦、⑧在周期表中的位置:第___周期,第_____族、第___周期,第____族
(3)①、③、④、⑥元素中的两种元素可形成含10个电子的分子,它们是_____、_____
(4)写出⑤的原子结构示意图_____________
(5)⑧的单质与氢氧化钠溶液反应的离子方程式_______________
【答案】H C N O 三 VIA 三 VIIA NH3 H2O  Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
【解析】
由元素在周期表中位置可知,①为H元素、②为C元素、③为N元素、④为O元素、⑤为Na元素、⑥为Al元素、⑦为Si元素、⑧为Cl元素。
(1)由元素在周期表中位置可知,①为H元素、②为C元素、③为N元素、④为O元素,故答案为:H;C;N;O;
(2)⑦为Si元素,位于周期表第三周期VIA族,⑧为Cl元素,位于周期表第三周期VIIA族,故答案为:三;VIA;三;VIIA;
(3)H元素与N、O元素形成的NH3、H2O为含10个电子的分子,故答案为:NH3;H2O;
(4)⑤为Na元素,原子结构示意图为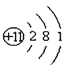 ,故答案为:
,故答案为: ;
;
(5)⑧为Cl元素,氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O。

 作业辅导系列答案
作业辅导系列答案【题目】阿魏酸化学名称为4羟基3甲氧基肉桂酸,可以做医药、保健品、化妆品原料和食品添加剂,结构简式为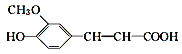 。在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团。下列试剂、现象、结论都正确的是( )
。在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团。下列试剂、现象、结论都正确的是( )
选项 | 试剂 | 现象 | 结论 |
A | 氯化铁溶液 | 溶液变蓝色 | 它含有酚羟基 |
B | 银氨溶液 | 产生银镜 | 它含有醛基 |
C | 碳酸氢钠溶液 | 产生气泡 | 它含有羧基 |
D | 溴水 | 溶液褪色 | 它含有碳碳双键 |
A. A B. B C. C D. D
【题目】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表是元素周期表的一部分。
H | He | ||||||
Li | Be | B | C | N | O | F | Ne |
Na | Mg | Al | Si | P | S | Cl | Ar |
请回答下列问题。
(1)非金属性最强的元素名称为___________,它位于元素周期表中的位置___________。
(2)硅元素的原子结构示意图是____________,其最高价氧化物是____________(填“酸性”或“碱性”)氧化物。
(3)硼酸(H3BO3)的酸性_________(填“>” 或“<”)碳酸(H2CO3)的酸性,说明你判断的理由:__________________________。
(4)NH3的电子式为________________,它属于____________(填“离子”或“共价”)化合物。NH3的还原性_________(填“>” 或“<”)PH3的还原性。
(5)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式______________。