题目内容
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下: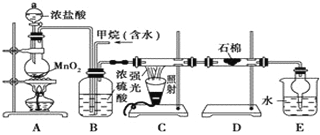
根据设计要求回答:
(1)A中发生反应的离子方程式为:______________________________
(2)B装置有三种功能:①均匀混合气;②干燥混合气体;③______________。
(3)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应≧________。
(4)E装置的作用是________________________________。
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出生成黑色小颗粒的化学方程式___________________________________。
(6)D装置中的石棉上放较多的KI粉末,其作用为________________________________。
(7)E装置除生成盐酸外,还含有有机物,从E中分离出有机物的最佳方法为________。
【答案】MnO2 + 4H++ 2Cl- ===Mn2+ + Cl2↑ + 2H2O 控制气流速度(或调整混合气的比例) 4 吸收氯化氢和防止倒吸 CH4+2Cl2![]() C+4HCl 除去未反应的氯气 分液
C+4HCl 除去未反应的氯气 分液
【解析】
A装置为制取氯气的发生装置,B装置可以除去水蒸气,可以混合甲烷和氯气,同时还可以通过产生气泡的快慢调节气体的流速;由于上述过程中产生的氯气和HCl均易导致大气污染,所以E的作用是吸收尾气。
(1)加热条件下,浓盐酸和二氧化锰反应生成氯化锰、氯气和水,反应的离子方程式为MnO2 + 4H++ 2Cl- ![]() Mn2+ + Cl2↑ + 2H2O,故答案为:MnO2 + 4H++ 2Cl-
Mn2+ + Cl2↑ + 2H2O,故答案为:MnO2 + 4H++ 2Cl- ![]() Mn2+ + Cl2↑ + 2H2O;
Mn2+ + Cl2↑ + 2H2O;
(2)B装置可以均匀混合气、干燥混合气体和控制气流速度(或调整混合气的比例),故答案为:控制气流速度(或调整混合气的比例);
(3)根据甲烷与氯气的反应可知欲获得较多的HCl,也就是使甲烷中的氢原子全部转化为HCl,此时消耗的氯气的物质的量至少是甲烷物质的量的4倍,故答案为:4;
(4)E能吸收氯化氢且能防止倒吸,所以E装置作用是吸收氯化氢和防止产生倒吸,故答案为:吸收氯化氢和防止倒吸;
(5)由题意可知,在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒为炭黑,说明光照条件下,氯气和甲烷发生取代反应生成黑色小颗粒碳和氯化氢,反应方程式为CH4+2Cl2![]() C+4HCl,故答案为:CH4+2Cl2
C+4HCl,故答案为:CH4+2Cl2![]() C+4HCl;
C+4HCl;
(6)氯气能将碘化钾氧化为碘单质,KI饱和溶液及KI粉末可除去过量的未反应氯气,故答案为:除去未反应的氯气;
(7)E装置中除了有盐酸生成外,还含有二氯甲烷、三氯甲烷和四氯化碳,二氯甲烷、三氯甲烷和四氯化碳不溶于水,能分层,可用分液分开,故答案为:分液。

【题目】已知H2(g)+Br2(g)=2HBr(g)ΔH=-Q kJmol-1,其他相关数据如下表:则Q的值为( )
H2(g) | Br2(g) | HBr(g) | |
1 mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 200 | 369 |
A. 102B. 260C. 230D. 404