题目内容
10.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项的事实不能说明上述观点的是( )| A. | 甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 | |
| B. | 乙烯能发生加成反应,而乙烷不能发生加成反应 | |
| C. | 苯与硝酸在加热的条件下发生取代反应,而甲苯在常温下就能与硝酸发生反应 | |
| D. | 苯酚能与氢氧化钠反应而乙醇不能 |
分析 A、苯、甲烷都不能使酸性高锰酸钾溶液褪色,甲苯可以,说明苯环对甲基的影响;
B、官能团不同导致,不是原子团间的相互影响导致;
C、甲苯与硝酸反应更容易,说明甲苯中苯环上H原子更活泼;
D、苯环对酚羟基影响的结果是酚羟基具有酸性.
解答 解:A、苯不能使酸性高锰酸钾溶液褪色,苯上没有可以被氧化的氢原子;甲苯能使高锰酸钾酸性溶液褪色,说明苯环的影响使侧链甲基易被氧化,故A不选;
B、乙烯中含有碳碳双键性质较活泼能发生加成反应,而乙烷中不含碳碳双键,性质较稳定,乙烷不能发生加成反应,所以乙烯和乙烷性质的不同是由于含有的化学键不同而导致的,故B选;
C、甲苯与硝酸反应更容易,说明甲基的影响使苯环上的氢变得活泼易被取代,故C不选;
D、在苯酚中,由于苯环对-OH的影响,酚羟基具有酸性,对比乙醇,虽含有-OH,但不具有酸性,故D不选;
故选B.
点评 本题主要考查有机物的结构与性质关系,难度中等,关键根据原子团所处的化学环境进行比较性质差异.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
18.有M、N、P、Q四块金属片,进行如下实验:
①M、N用导线相连后,同时插入硫酸铜溶液中,N极变粗
②P、Q用导线相连后,同时浸入稀H2SO4中,Q是电子流入的一极
③M、P相连后,同时浸入稀H2SO4,P极产生大量气泡
④N、Q相连后,同时浸入稀H2SO4中,Q极发生氧化反应
则四种金属的活动性顺序为( )
①M、N用导线相连后,同时插入硫酸铜溶液中,N极变粗
②P、Q用导线相连后,同时浸入稀H2SO4中,Q是电子流入的一极
③M、P相连后,同时浸入稀H2SO4,P极产生大量气泡
④N、Q相连后,同时浸入稀H2SO4中,Q极发生氧化反应
则四种金属的活动性顺序为( )
| A. | M>N>P>Q | B. | M>P>Q>N | C. | N>Q>P>M | D. | P>M>N>Q |
5.五种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
请回答下列问题:
(1)请写出元素名称:X碳Y氮Z磷W硫M氯
(2)元素X位于周期表中第二周期ⅣA族;
(3)Y的最高价氧化物的水化物化学式为HNO3;
(4)元素Z可以形成多种单质,其中最常见两种名称分别是白磷、红磷;
(5)W原子的电子式是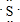 ;它的气态氢化物的结构式为H-S-H.
;它的气态氢化物的结构式为H-S-H.
(6)M的单质与水反应的化学方程式是Cl2+H2O═HCl+HClO.
| X | Y | ||
| Z | W | M |
(1)请写出元素名称:X碳Y氮Z磷W硫M氯
(2)元素X位于周期表中第二周期ⅣA族;
(3)Y的最高价氧化物的水化物化学式为HNO3;
(4)元素Z可以形成多种单质,其中最常见两种名称分别是白磷、红磷;
(5)W原子的电子式是
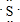 ;它的气态氢化物的结构式为H-S-H.
;它的气态氢化物的结构式为H-S-H.(6)M的单质与水反应的化学方程式是Cl2+H2O═HCl+HClO.
15.在 分子中,处于同一平面上的碳原子数最多可能有( )
分子中,处于同一平面上的碳原子数最多可能有( )
 分子中,处于同一平面上的碳原子数最多可能有( )
分子中,处于同一平面上的碳原子数最多可能有( )| A. | 6个 | B. | 8个 | C. | 10个 | D. | 12个 |
2.下列有关说法正确的是( )
| A. | 天然蛋白质水解的最终产物只有一种α氨基酸 | |
| B. | 甘油常应用于化妆品的生产,是因为其具有吸水性 | |
| C. | 淀粉、纤维素、油脂都是高分子化合物 | |
| D. | 苯酚和甲醛都有毒,故不能直接或间接用于制备消毒剂 |
19.下列说法正确的是( )
| A. | 金属元素和非金属元素间形成的化学键一定是离子键 | |
| B. | 伴有能量变化的物质变化不一定是化学变化 | |
| C. | 可逆反应达到化学平衡时,正逆反应速率都为0 | |
| D. | 通过化学变化可以实现1H与2H间的相互转化 |
20.“塑料袋--想说爱你不容易!”自1902年10月24日奥地利科学家马克斯•舒施尼发明它以来,也只有短短的一百多年时间.这些花花绿绿、大大小小的塑料袋,不仅破坏城市景观,对环境的危害也是极惊人的.2008年6月1日起,根据国务院要求,所有超市、商场、集贸市场等商品零售场所实行塑料购物袋有偿使用.下列说法正确的是( )
| A. | 聚丙烯塑料的结构简式为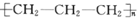 | |
| B. | 聚氯乙烯塑料单体的电子式为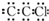 | |
| C. | 塑料购物袋的生产原料需要消耗大量木材 | |
| D. | 聚乙烯中含碳质量分数与其单体的含碳质量分数相同 |