题目内容
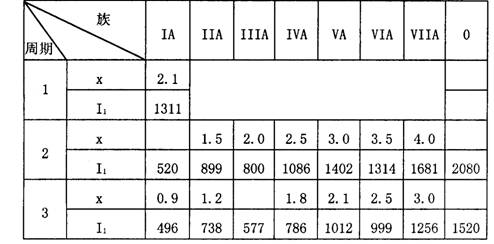
下列各元素中,原子半径依次增大的是( )
分析:根据元素周期律知,同一周期,元素的原子半径随着原子序数的增大而减小;同一主族,元素的原子半径随着原子序数的增大而增大,据此分析解答.
解答:解:A、Na、Mg、Al属于同一周期,且Na、Mg、Al的原子序数依次增大,所以原子半径依次减小,故A错误;
B、N、O、F属于同一周期,且N、O、F的原子序数依次增大,所以原子半径依次减小,故B错误;
C、P、Si、Al属于同一周期,且P、Si、Al的原子序数依次减小,所以原子半径依次增大,故C正确;
D、C、Si属于同一主族,C的原子序数小于Si的,所以碳的原子半径小于硅的原子半径;Si、P属于同一周期,且
Si的原子序数小于P的原子序数,所以Si的原子半径大于P的原子半径,P的电子层数比碳的多,所以P的原子半径大于C的原子半径,C、Si、P的原子半径从小到大的顺序为C、P、Si,故D错误;
故选C.
B、N、O、F属于同一周期,且N、O、F的原子序数依次增大,所以原子半径依次减小,故B错误;
C、P、Si、Al属于同一周期,且P、Si、Al的原子序数依次减小,所以原子半径依次增大,故C正确;
D、C、Si属于同一主族,C的原子序数小于Si的,所以碳的原子半径小于硅的原子半径;Si、P属于同一周期,且
Si的原子序数小于P的原子序数,所以Si的原子半径大于P的原子半径,P的电子层数比碳的多,所以P的原子半径大于C的原子半径,C、Si、P的原子半径从小到大的顺序为C、P、Si,故D错误;
故选C.
点评:本题考查了原子半径大小的半径,难度不大,注意电子层结构相同的离子半径大小的比较方法.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
 (2012?武汉模拟)[化学一选修 3:物质结构与性质]有U、V、W、X、Y、Z 六种前四周期元素,原子序数依次增大,其相关信息如下表:
(2012?武汉模拟)[化学一选修 3:物质结构与性质]有U、V、W、X、Y、Z 六种前四周期元素,原子序数依次增大,其相关信息如下表: