题目内容
(14分)现有X、Y、Z、W、R五种元素,其中前四种为短周期主族元素。X原子的最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价的代数和为6;X、Z同主族,W与X、Y均不同周期,R2+的价电子排布式为3d5。
(1)R元素在周期表中的位置 ;W2X2的电子式 。
(2)X、Y、Z的最低价氢化物中:沸点最高的是 (填化学式);共价键键能最小的是 ;X、Y、Z的杂化类型 (填相同或不相同)。
(3)若R的晶体中每个晶胞平均含有2个R原子,请在下图晶胞中用?标出未画出的R原子。

(4)将1.19g ZXY2溶于100ml水中发生非氧化还原反应,生成2种酸,反应方程式为 ;所得溶液中阴离子浓度由大到小的顺序是 。
(1)R元素在周期表中的位置 ;W2X2的电子式 。
(2)X、Y、Z的最低价氢化物中:沸点最高的是 (填化学式);共价键键能最小的是 ;X、Y、Z的杂化类型 (填相同或不相同)。
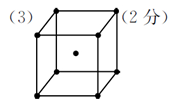
(3)若R的晶体中每个晶胞平均含有2个R原子,请在下图晶胞中用?标出未画出的R原子。

(4)将1.19g ZXY2溶于100ml水中发生非氧化还原反应,生成2种酸,反应方程式为 ;所得溶液中阴离子浓度由大到小的顺序是 。
(14分)
(1)第四周期VIIB (2分)
(2)H2O(1分) H2S(1分)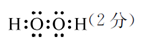 相同(2分)
相同(2分)
(4)SOCl2+2H2O=2HCl+H2SO3(2分)
c(Cl?) > c(HSO3?) > c(SO32?) > c(OH?) (2分)
(1)第四周期VIIB (2分)
(2)H2O(1分) H2S(1分)
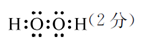 相同(2分)
相同(2分)
(4)SOCl2+2H2O=2HCl+H2SO3(2分)
c(Cl?) > c(HSO3?) > c(SO32?) > c(OH?) (2分)
试题分析:X原子的最外层电子数是核外电子层数的3倍,则X为O元素;X、Z同主族,且为短周期元素,则Z为S元素;Y的最高正价与最低负价的代数和为6,则Y为Cl元素;W与X、Y均不同周期,W为H元素;R2+的价电子排布式为3d5,故R为Mn元素。
(1)R为Mn元素,原子序数为25,在周期表中位于第四周期VIIB;W2X2为H2O2电子式为:
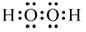
(2)X、Y、Z的最低价氢化物分别为H2O、HCl、H2S,因为H2O分子间能形成氢键,作用力更强,所以H2O的沸点最高;O、Cl、S元素非金属性最弱的是S元素,所以H2S共价键键能最小;O、Cl、S的杂化类型都是sp3杂化,杂化类型相同。
(3)每个晶胞平均含有2个R原子,图中已标出的原子位于体心,则未标出的R原子应在立方体的8个顶点上。
(4)ZXY2为SOCl2与水发生非氧化还原反应,生成2种酸为HCl和H2SO3,所以化学方程式为:SOCl2+2H2O=2HCl+H2SO3;H2SO3为中强酸,第一步电离大于第二步电离,所以阴离子浓度由大到小的顺序是:c(Cl?) > c(HSO3?) > c(SO32?) > c(OH?)

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目




