题目内容
构成原子的微粒——电子、质子和中子的基本数据:
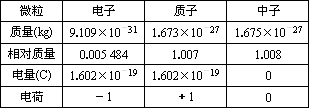
请根据表中所列数据讨论:
①在原子中,质子数、核电荷数和核外电子数之间存在着什么关系?为什么?
②原子的质量主要由哪些微粒决定?
答案:
解析:
解析:
|
①因为质子与核外电子所带的电量相等、电性相反,中子不带电,原子是电中性的,故质子所带的总电量跟核外电子所带的总电量相等,即质子数与核外电子数相等.一个质子带一个单位的正电荷,故质子数等于核电荷数.综合分析即可得出质子数=核电荷数=核外电子数. ②因电子的质量比质子和中子的质量小得多,可以忽略不计.因此原子的质量主要集中在原子核上,而原子核又是由质子和中子构成的.故原子的质量主要由质子和中子决定. |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
构成物质的微粒种类及相互间的作用力是决定物质表现出何种物质性质的主要因素.
(1)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体类型为______;
(2)氢键作用常表示为“A…HB“,其中A\B为电负性很强的一类原子,如______
(列举三种.X、Y两种物质和部分物质性质如下表,二者物质性质有差异的主要原因是______
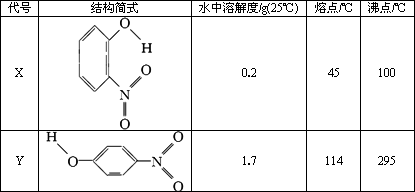
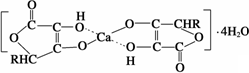
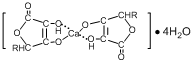
(3)钙是人体所需的重要元素之一,有一种补钙剂--抗坏血酸的组成为Ca(C6H7O6)?2H2O]其结构示意图如下: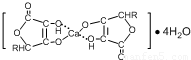
该物质中存在的化学键类型包括______(填字母)
A.金属键B.离子键C.共价键D.配位键
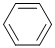
(4)①CH2=CH2、②CH≡CH、③ ④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是______.这四种分子中碳原子采取sp2杂化的是______(填序号).
④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是______.这四种分子中碳原子采取sp2杂化的是______(填序号).
(1)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体类型为______;
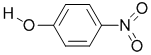
| 代号 | 结构简式 | 水中溶解度/g(25℃) | 熔点/℃ | 沸点/℃ |
| X |  | 0.2 | 45 | 100 |
| Y |  | 1.7 | 114 | 295 |
(列举三种.X、Y两种物质和部分物质性质如下表,二者物质性质有差异的主要原因是______
(3)钙是人体所需的重要元素之一,有一种补钙剂--抗坏血酸的组成为Ca(C6H7O6)?2H2O]其结构示意图如下:

该物质中存在的化学键类型包括______(填字母)
A.金属键B.离子键C.共价键D.配位键
(4)①CH2=CH2、②CH≡CH、③
 ④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是______.这四种分子中碳原子采取sp2杂化的是______(填序号).
④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是______.这四种分子中碳原子采取sp2杂化的是______(填序号).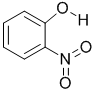
 ④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是
④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是