题目内容
3.下列物质中含原子数最多的是( )| A. | 0.4mol O2 | B. | 3.01×1022个CO2 分子 | ||
| C. | 4℃时,5.4mL水 | D. | 标准状况下,11.2L氩 |
分析 根据各物质所含原子的物质的量判断.
A.原子物质的量为氧气分子2倍;
B.根据n=$\frac{N}{{N}_{A}}$计算个CO2 物质的量,含有原子物质的量为个CO2 分子的3倍;
C.根据m=ρV计算水的质量,再根据n=$\frac{m}{M}$计算水的物质的量,含有原子物质的量为水的3倍;
D.据n=$\frac{V}{{V}_{m}}$计算氩气的物质的量,氩气为单原子分子.
解答 解:A.0.4molO2所含原子的物质的量为0.4mol×2=0.8mol;
B.3.01×1022个CO2 分子的物质的量为0.05mol,所含的原子的总的物质的量为0.5mol×3=0.15mol;
C.15mol5.4ml水的质量为5.4ml×1g/ml=5.4g,其物质的量为$\frac{5.4g}{18g/mol}$=0.3mol,所含原子的物质的量为0.3mol×3=0.9mol;
D.标准状况下,11.2L氩的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,氩气为单原子分子,故含有N氩原子为0.5mol.
所以含原子数目大小顺序为C>A>D>B,
故选C.
点评 本题考查物质的量有关计算,难度较小,旨在考查学生对化学常用计量的理解,注意稀有气体为单原子分子.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列对难溶电解质的溶解平衡的叙述,错误的是( )
| A. | 难溶电解质的溶解平衡是一种动态平衡 | |
| B. | 达到溶解平衡时,沉淀的速率和溶解的速率相等,溶液中离子的浓度保持不变 | |
| C. | 达到溶解平衡时,溶液中各种离子的浓度不一定相等 | |
| D. | 达到溶解平衡时,再加入该难溶电解质,将促进其溶解 |
14.从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平.图表示了三种金属被人类开发利用的大致年限,之所以有先后,主要取决于( )
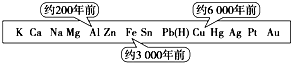

| A. | 金属的导电性强弱 | B. | 金属在地壳中的含量多少 | ||
| C. | 金属的活动性大小 | D. | 金属的化合价高低 |
11.下列有关钠和镁的说法中,正确的是( )
| A. | 电解NaCl溶液可以得到金属钠 | |
| B. | 金属钠在Cl2中燃烧产生黄色火焰得到黄色固体 | |
| C. | 金属镁着火,可用二氧化碳灭火 | |
| D. | 金属镁燃烧时发出耀眼的白光,因此常用来制造信号弹和焰火 |
8.下列有关化学用语表示正确的是( )
| A. | ${\;}_{8}^{18}$O2-离子结构示意图: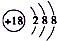 | B. | 四氯化碳分子的比例模型: | ||
| C. | 次氯酸的电子式: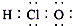 | D. | 中子数为16的硫离子:${\;}_{16}^{32}$S2- |
15.将a g 含NaOH样品溶解在b mL 0.1mol/L的硫酸中(杂质不反应),再加入c mL 0.1mol/L的氢氧化钡溶液,反应后所得溶液恰好呈中性,则样品中NaOH的纯度是( )
| A. | $\frac{b-c}{125a}$×100% | B. | $\frac{b-2c}{125a}$×100% | C. | $\frac{b-c}{250a}$×100% | D. | $\frac{8b-8c}{a}$×100% |
12.化学与生产、生活、社会密切相关,下列有关说法中错误的是( )
| A. | 糖类、油脂、蛋白质、无机盐和水均是动物性和植物性食物中的基本营养物质 | |
| B. | 84消毒液可用于环境消毒,医用酒精可用于皮肤消毒,其原因在于可以使病毒和细菌体内的蛋白变性 | |
| C. | 加快开发太阳能、氢能等新能源有利于降低空气中PM2.5的含量 | |
| D. | “忽闻还上有仙山,山在虚无缥缈间”的海市蜃楼现象的形成与胶体性质有关 |
18.一定条件下,某反应达到化学平衡时,下列说法错误的是( )
| A. | 反应停止了 | B. | 各物质的浓度不再改变 | ||
| C. | 正反应速率等于逆反应速率 | D. | 该反应达到最大限度 |