题目内容
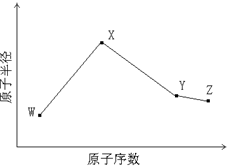 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为14,中子数为7;X的离子与NH4+具有相同的质子、电子数目; W与Y的氧化物均能导致酸雨的形成;Z的非金属性在同周期主族元素中最强.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为14,中子数为7;X的离子与NH4+具有相同的质子、电子数目; W与Y的氧化物均能导致酸雨的形成;Z的非金属性在同周期主族元素中最强.(1)Y在周期表中的位置是
(2)用电子式解释X与W能形成化合物X3W的原因
(3)X3W遇水可释放出使酚酞溶液变红的气体A,化学方程式是
(4)用惰性电极电解化合物XZ溶液从阴极释放出气体B,反应的离子方程式是
(5)已知W的单质与气体B在一定条件下可形成气体A,即:W2(g)+3B (g)?2A(g)△H=-92.4kJ?mol-1
在某温度时,一个容积固定的密闭容器中,发生上述反应.在不同时间测定的容器内各物质的浓度如下表:
| 时间 | 浓度(mol/L) | ||
| c(W2) | c(B) | c(A) | |
| 第0min | 4.0 | 9.0 | 0 |
| 第10min | 3.8 | 8.4 | 0.4 |
| 第20min | 3.4 | 7.2 | 1.2 |
| 第30min | 3.4 | 7.2 | 1.2 |
| 第40min | 3.6 | 7.8 | 0.8 |
②反应在第10min改变了反应条件,改变的条件可能是
a.更新了催化剂 b.升高温度 c.增大压强 d.增加B的浓度
③若反应从第30min末又发生了一次条件改变,改变的反应条件可能是
a.更新了催化剂 b.升高温度 c.增大压强 d.减小A的浓度.
分析:W、X、Y、Z是四种常见的短周期元素,W的一种核素的质量数为14,中子数为7,质子数为14-7=7,故W为氮元素;X的离子与NH4+具有相同的质子、电子数目,X的质子数为11,故X为Na元素;由图可知,X、Y、Z的原子序数依次增大,都处于第三周期,Y的氧化物均能导致酸雨的形成,故Y为硫元素;Z的非金属性在同周期主族元素中最强,故Z为Cl元素,据此解答.
解答:解:W、X、Y、Z是四种常见的短周期元素,W的一种核素的质量数为14,中子数为7,质子数为14-7=7,故W为氮元素;X的离子与NH4+具有相同的质子、电子数目,X的质子数为11,故X为Na元素;由图可知,X、Y、Z的原子序数依次增大,都处于第三周期,Y的氧化物均能导致酸雨的形成,故Y为硫元素;Z的非金属性在同周期主族元素中最强,故Z为Cl元素,
(1)Y为硫元素,原子有3个电子层,最外层电子数为6,处于周期表中第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(2)用电子式表示Na3N的形成为: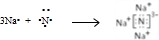 ,故答案为:
,故答案为: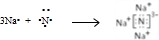 ;
;
(3)Na3N遇水可释放出使酚酞溶液变红的气体A,A为碱性气体,故A为NH3,由水解原理可知,还生成NaOH,反应化学方程式是:Na3N+3H2O=NH3↑+3NaOH,
故答案为:Na3N+3H2O=NH3↑+3NaOH;
(4)用惰性电极电解化合物NaCl溶液从阴极释放出气体B,B为H2,电解NaCl溶液生成氢气、氯气、氢氧化钠,反应的离子方程式是:2Cl-+2H2O
Cl2↑+H2↑+2OH-,故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-;
(5)①相同时间内同种物质表示的速率之比等于浓度变化量之比,故Cl2的平均反应速率v(0min~10min)/v(10min~20min)=
=
,
故答案为:
;
②由表中数据可知,10min~20min的速率比0min~10min速率快,10min时反应未到达平衡,反应进行向正反应进行,20min与10min相比,W2、B、A的浓度变化量为分别为0.2mol/L、0.6mol/L、0.4mol/L,等于化学计量数之比,故不可能为增大某一物质浓度,增大压强反应混合物的浓度都应增大,W2、B 浓度降低,故不可能为增大压强,故10min时改变条件应是更新了催化剂或升高温度加快反应速率,故答案为:ab;
③由表中数据可知,20min时反应到达平衡,30min末又发生了一次条件改变,由40min时各组分的浓度可知,平衡向逆反应进行,40min与30min相比,W2、B、A的浓度变化量为分别为0.2mol/L、0.6mol/L、0.4mol/L,等于化学计量数之比,故不可能为减小某一反应物的浓度,也不可能是增大A的浓度,降低压强平衡向逆反应移动,W2、B的浓度也应该降低,故不可能为降低压强,使用催化剂,不影响平衡移动,该反应正反应为放热反应,故30min时改变条件应是升高温度,故答案为:b.
(1)Y为硫元素,原子有3个电子层,最外层电子数为6,处于周期表中第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(2)用电子式表示Na3N的形成为:
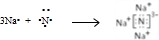 ,故答案为:
,故答案为: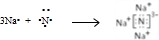 ;
;(3)Na3N遇水可释放出使酚酞溶液变红的气体A,A为碱性气体,故A为NH3,由水解原理可知,还生成NaOH,反应化学方程式是:Na3N+3H2O=NH3↑+3NaOH,
故答案为:Na3N+3H2O=NH3↑+3NaOH;
(4)用惰性电极电解化合物NaCl溶液从阴极释放出气体B,B为H2,电解NaCl溶液生成氢气、氯气、氢氧化钠,反应的离子方程式是:2Cl-+2H2O
| ||
| ||
(5)①相同时间内同种物质表示的速率之比等于浓度变化量之比,故Cl2的平均反应速率v(0min~10min)/v(10min~20min)=
| 4mol/L-3.8mol/L |
| 3.8mol/L-3.4mol/L |
| 1 |
| 2 |
故答案为:
| 1 |
| 2 |
②由表中数据可知,10min~20min的速率比0min~10min速率快,10min时反应未到达平衡,反应进行向正反应进行,20min与10min相比,W2、B、A的浓度变化量为分别为0.2mol/L、0.6mol/L、0.4mol/L,等于化学计量数之比,故不可能为增大某一物质浓度,增大压强反应混合物的浓度都应增大,W2、B 浓度降低,故不可能为增大压强,故10min时改变条件应是更新了催化剂或升高温度加快反应速率,故答案为:ab;
③由表中数据可知,20min时反应到达平衡,30min末又发生了一次条件改变,由40min时各组分的浓度可知,平衡向逆反应进行,40min与30min相比,W2、B、A的浓度变化量为分别为0.2mol/L、0.6mol/L、0.4mol/L,等于化学计量数之比,故不可能为减小某一反应物的浓度,也不可能是增大A的浓度,降低压强平衡向逆反应移动,W2、B的浓度也应该降低,故不可能为降低压强,使用催化剂,不影响平衡移动,该反应正反应为放热反应,故30min时改变条件应是升高温度,故答案为:b.
点评:本题考查位置结构性质关系、处于化学用语、化学反应速率计算、化学平衡的影响因素等,难度较大.(5)中②③注意根据浓度变化结合外界条件影响解答,②中增大压强为易错点,只考虑速率加快,容易忽略浓度变化.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z是
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z是
 (2011?安徽)W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
(2011?安徽)W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大. (2013?济宁一模)W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是( )
(2013?济宁一模)W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是( ) W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.(以下答案的W、X、Y、Z必须用相应的元素符号代替)
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.(以下答案的W、X、Y、Z必须用相应的元素符号代替)