题目内容
X、Y、Z、M、N 代表五种金属。有以下化学反应:
①水溶液中:X+Y2+=X2++Y ②Z+2H2O(冷)=Z(OH)2+H2↑
③M、N 为电极与 N 盐溶液组成原电池,发生的电极反应为:M-2e— =M2+
④Y 可以溶于稀 H2SO4中,M 不被稀 H2SO4氧化. 则这五种金属的活泼性由弱到强的顺序是
| A.M<N<Y<X<Z | B.N<M<X<Y<Z |
| C.N<M<Y<X<Z | D.X<Z<N<M<Y |
C
解析试题分析:①水溶液中:X+Y2+=X2++Y,根据还原性强弱顺序,还原剂的还原性强于还原产物的还原性,X>Y,②Z+2H2O(冷)=Z(OH)2+H2↑,能和冷水反应,说明Z非常活泼,③M、N 为电极与 N 盐溶液组成原电池,发生的电极反应为:M-2e— =M2+,M作负极说明M>N,④Y 可以溶于稀 H2SO4中,M 不被稀 H2SO4氧化,说明Y>M,联立不等式关系可以得出结论,答案选C。
考点:考查金属性强弱的比较

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
同主族常见的三种元素X、Y、Z,它们最高价氧化物对应水化物的酸性强弱顺序为:HXO4<HYO4<HZO4,下列判断不正确的是
| A.Y单质可以在海水中提取 | B.离子半径: X->Y- |
| C.气态氢化物稳定性:HX<HZ | D.单质氧化性: Y>Z |
下列各组关系正确的是:
| A.原子半径 N<P<S | B.稳定性 NH3<H2O<HF |
| C.碱性 NaOH>KOH | D.酸性 H3AsO4>H2SeO4>HBrO4 |
元素X形成的简单离子与钙离子的核外电子排布相同,且X的简单离子半径大于氯离子的半径,则X元素为
| A.Mg | B.S | C.Ar | D.K |
柳州的龙江河铬污染事故再一次令人触目惊心,环境保护刻不容缓。下列关于铬的一种原子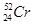 说法正确的是
说法正确的是
A.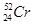 与 与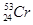 互为同素异形体 互为同素异形体 |
B.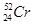 含有24个中子 含有24个中子 |
C.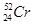 与 与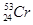 互为同位素,物理性质、化学性质均相同 互为同位素,物理性质、化学性质均相同 |
D.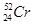 中子数比电子数多4个 中子数比电子数多4个 |
以下对粒子结构或性质的叙述正确的是( )
| A.两种微粒,若核外电子排布完全相同,则化学性质一定相同 |
| B.由单原子形成的离子,一定具有稀有气体元素原子核外电子排布 |
| C.阴离子的核外电子排布一定与上一周期稀有气体原子核外排布相同 |
| D.两原子,如果核外电子排布相同,则一定属于同一种元素 |
目前科学家普遍认为,质子和中子都是由被称为u夸克和d夸克的两类夸克构成,u夸克带电量为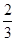 e,d夸克带电量为-
e,d夸克带电量为-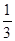 e,e为基元电荷,下列论断中可能正确的是( )
e,e为基元电荷,下列论断中可能正确的是( )
| A.质子是由1个u夸克和1个d夸克构成,中子是由1个u夸克和2个d夸克构成的 |
| B.质子是由2个u夸克和1个d夸克构成的,中子是由1个u夸克和2个d夸克构成的 |
| C.质子是由1个u夸克和2个d夸克构成的,中子是由2个u夸克和1个d夸克构成的 |
| D.质子是由2个u夸克和1个d夸克构成的,中子是由1个u夸克和1个d夸克构成的 |
下列有关结构和性质的说法正确的是
A.元素铯的两种核素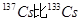 多4个质子 多4个质子 |
| B.P、S、C1得电子能力和最高价氧化物对应水化物的酸性均依次增强 |
| C.元素原子的最外层电子数越多,越容易得电子 |
| D.从上到下,第VIIA族元素氢化物的热稳定性和还原性均依次减弱 |
下表为周期表的一部分,有关短周期X、Y、Z、R四种元素叙述正确的是:
| A.热稳定性:Y的气态氢化物<Z的气态氢化物 |
| B.X的最高价氧化物对应水化物的酸性比Y的强 |
| C.X元素的单质能与所有强酸发生反应放出H2 |
| D.R元素的单质化学性质活泼 |