题目内容
17.据报道,反式脂肪酸目前被广泛添加于加工食品中,而反式脂肪酸会导致心脏病和糖尿病等疾病.已知某种反式脂肪酸的结构简式为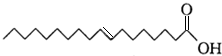 ,下列判断不正确的是( )
,下列判断不正确的是( )| A. | 该物质与丙烯酸互为同系物 | |
| B. | 该物质的分子式为C18H34O2 | |
| C. | 该物质易溶于水,在空气中不易变质 | |
| D. | 该物质的碳链含有锯齿形结构 |
分析 该物质中含有碳碳双键和羧基,所以具有烯烃和羧酸的性质,能发生加成反应、加聚反应、氧化反应、取代反应、酯化反应、中和反应,据此分析解答.
解答 解:A.丙烯酸结构简式为CH2=CHCOOH,该物质结构和丙烯酸相似,比丙烯酸多15个-CH2原子团,所以与丙烯酸是同系物,故A正确;
B.根据结构简式知,分子式为C18H34O2,故B正确;
C.亲水基相对分子质量较小,所以该物质难溶于水,含不饱和键,在空气中易被氧化,故C错误;
D.根据键线式知,该物质的碳链含有锯齿形结构,故D正确;
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重考查基本概念、物质性质和结构关系,易错选项是D.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
7.生活中的某些问题常常涉及化学知识.下列叙述错误的是( )
| A. | 用聚乳酸塑料代替聚乙烯塑料可减少白色污染 | |
| B. | 煤油、“乙醇汽油”、“生物柴油”都是碳氢化合物 | |
| C. | 为防治碘缺乏病,在食用盐中添加适量的碘酸钾 | |
| D. | 甘油可用作护肤保湿剂 |
5.某有机物能使溴水褪色,也能在一定条件下发生水解生成两种有机物,还能发生加聚反应生成高分子化合物,则此有机物中一定含有下列基团的组合是( )
①-CH3;②-OH;③-Cl;④-CHO;⑤-C2H3;⑥-COOH;⑦-COOCH3.
①-CH3;②-OH;③-Cl;④-CHO;⑤-C2H3;⑥-COOH;⑦-COOCH3.
| A. | ①③ | B. | ②⑥ | C. | ⑤⑦ | D. | ④⑤ |
9.下列表示式正确的是( )
| A. | 氨分子的电子式 | B. | 氢氧根离子的电子式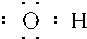 | ||
| C. | 乙酸的结构简式 C2H4O2 | D. | 苯的实验式 C6H6 |
7.四种常见元素的性质或结构信息如下表,试根据信息回答有关问题.
(1)写出C原子的基态电子排布式[Ar]3d104s1.D中成对电子数与未成对电子数之比为2:1.
(2)A元素的氢化物的沸点比同主族相邻元素氢化物沸点高(填“高”或“低”),其原因氨气分子之间存在氢键.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是CO2为分子晶体,SiO2是原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,该配合物中存在的化学键类型是ABD.(填字母)
A、离子键 B、共价键 C、金属键 D、配位键 E、分子间作用力
(5)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“O”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.
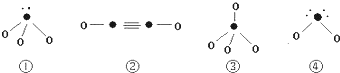
则在以上分子中,中心原子采用sp3杂化的是①③④;属于极性分子的是①④.(以上均填写序号).在②的分子中有3个σ键和2个π键.
| 元素 | A | B | C | D |
| 性质 结构 信息 | 基态原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(2)A元素的氢化物的沸点比同主族相邻元素氢化物沸点高(填“高”或“低”),其原因氨气分子之间存在氢键.
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是CO2为分子晶体,SiO2是原子晶体.
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,该配合物中存在的化学键类型是ABD.(填字母)
A、离子键 B、共价键 C、金属键 D、配位键 E、分子间作用力
(5)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“O”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.
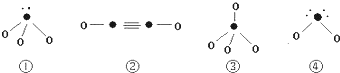
则在以上分子中,中心原子采用sp3杂化的是①③④;属于极性分子的是①④.(以上均填写序号).在②的分子中有3个σ键和2个π键.
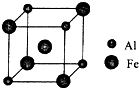 过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.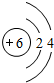 ,B与C形成的化合物的电子式为
,B与C形成的化合物的电子式为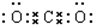 .
.