题目内容
9.碳,氮,硅的最高价酸性氧化物的化学式分别是CO2、N2O5、SiO2.分析 酸性氧化物是能和碱反应生成盐和水的氧化物,碳,氮,硅的最高价分别是+4、+5、+4,根据氧化物的组成特点结合化合价规则来书写化学式.
解答 解:碳,氮,硅的最高价分别是+4、+5、+4,氧化物的组成特点:含有两种元素,一种是氧元素,氧元素的化合价是-2价,根据化合价规则,碳,氮,硅的最高价酸性氧化物的化学式分别是CO2、N2O5、SiO2.
故答案为:CO2;N2O5;SiO2.
点评 本题主要考查的是酸性氧化物的概念知识,涉及化学式的推断与书写,难度不大,注意整理.

练习册系列答案
相关题目
4.在100mL含等物质的量HBr和H2SO3的溶液里通入标准状况224mlCl2,有一半Br-变为Br2.则反应后溶液中SO42-的浓度等于(假设反应前后溶液体积忽略不计)( )
| A. | 0.08mol/L | B. | 0.0018mol/L | C. | 0.075mol/L | D. | 0.0075mol/L |
14.将甲乙两种有机物组成的混合物进行分离,已知甲乙的某些特征如下:
则应采取的分离方法是( )
| 物质 | 密度/(g•mL-1) | 沸点 | 水溶性 | 溶解性 |
| 甲 | 0.893 | 78.5℃ | 溶 | 溶于乙 |
| 乙 | 1.220 | 100.7℃ | 溶 | 溶于甲 |
| A. | 蒸馏 | B. | 升华 | C. | 分液 | D. | 过滤 |
20.X、Y、Z、W是原子序数依次增大的前20号元素,X、Y同周期,Y、Z同主族,X原子的最外层电子数为内层电子数的2倍,Y是地壳中含量最多的元素,W为金属元素,且原子中无成单电子,下列叙述不正确的是( )
| A. | Z的离子半径比W的离子半径小 | |
| B. | 第一电离能:X<Y | |
| C. | Y的氢化物的沸点比Z的氢化物沸点高 | |
| D. | 室温时,WXY3在纯水存在沉淀溶解平衡 |
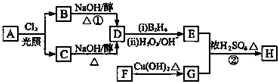
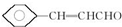 .
.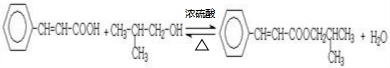 ;
;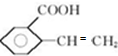 、
、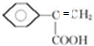 .
.
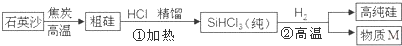

 ;HCl.
;HCl.