题目内容
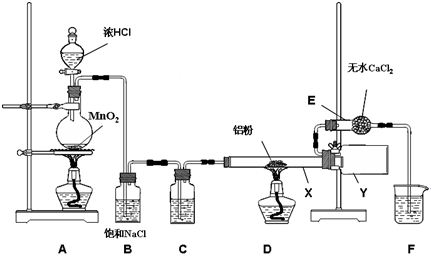
17.实验室可用氯气和金属铁反应制备无水三氯化铁,该化合物呈红棕色、易与水发生较剧烈的化学反应,100度左右时易升华.如图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置则不同,分别如1、2所示.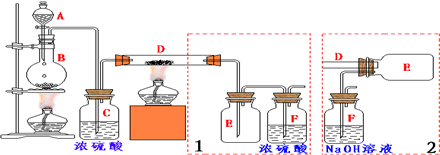
(1)写出B中制取Cl2的反应化学方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)当D中有充满黄绿色气体现象时再点燃D处酒精灯的比较合适.
(3)装置1 和装置2的都有缺点,如果选用2装置完成实验,则必须采取的改进措施是在E、F之间加入一个装有浓硫酸的洗气瓶.
分析 实验室用氯气和金属铁反应制备无水三氯化铁:A为分液漏斗盛放浓盐酸,B为圆底烧瓶盛放二氧化锰,浓盐酸和二氧化锰加热制取氯气:4HCl(浓)+MnO2?$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑,制取的氯气中含有水蒸气,C装置浓硫酸进行干燥氯气,装置D,在加热条件下,铁和氯气反应,反应方程式为2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3,制得氯化铁.
(1)实验室用氯气和铁反应制取氯化铁,所以首先必须制取氯气,实验室常用浓盐酸和二氧化锰加热制取氯气,加热条件下,浓盐酸和二氧化锰反应生成氯化锰、氯气和水;
(2)AB处是制取氯气,D是氯气和铁反应,所以先点B处酒精灯,B中的反应进行一段时间后,看到黄绿色气体充满装置,再开始加热D使制取的Cl2排尽装置内的空气,防止铁被空气中氧气氧化;
(3)装置(Ⅰ)的主要缺点是导管易被产品堵塞,有毒气体应该有尾气处理装置;装置(Ⅱ)的主要缺点是:尾气处理装置中有水,导致氯化铁易潮解.
解答 解:(1)浓盐酸与二氧化锰在加热条件下生成氯气、氯化锰和水,化学方程式为4HCl(浓)+MnO2?$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑,
故答案为:4HCl(浓)+MnO2?$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑;
(2)D是氯气和铁反应,防止氧气和铁反应生成铁的氧化物而产生杂质,所以D中的反应开始前,必须排除装置中的空气,其方法是B中的反应进行一段时间后,看到共绿色气体充满装置,再开始加热D,
故答案为:充满黄绿色气体;
(3)装置(Ⅰ)的主要缺点是:导气管口较小,D装置中的固体物质易堵塞导管口;氯气是有毒气体,不能直接排空,否则会污染环境,所以应该有一个尾气处理装置,装置(Ⅱ):装置中有尾气处理装置,但尾气处理装置中是水溶液,会导致E中有水蒸气,会导致氯化铁产品易潮解,所以为防止氯化铁潮解,在瓶E和F之间连接装有干燥剂的装置,
故答案为:在E、F之间加入一个装有浓硫酸的洗气瓶.
点评 本题以氯化铁的制备为载体,考查了氯气的制备和性质的检验、实验装置的优劣分析,解题关键理在于明确实验原理和目的及各装置的作用,题目难度中等.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案(1)将PM2.5样本用蒸馏水处理制成待测试样,若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)为减少SO2的排放,可洗涤含SO2的烟气,下列物质可作洗涤剂的是ab(填字母).
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是吸热反应,温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g).
已知该反应的△H>0,简述该设想能否实现的依据:△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
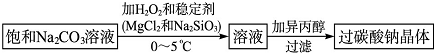
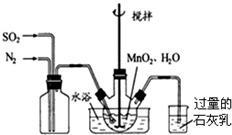 高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下: