题目内容
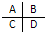
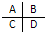
 如图是某短周期主族元素最高价氧化物水化物某相同浓度稀溶液与原子半径的关系示意图,则下列说法正确的是( )
如图是某短周期主族元素最高价氧化物水化物某相同浓度稀溶液与原子半径的关系示意图,则下列说法正确的是( )| A、原子序数:W>Z>X | B、气态氢化物的稳定性:N>R | C、Y和W形成共价化合物 | D、X和Z两者最高价氧化物对应的水化物能相互反应 |
分析:同周期元素从左到右元素的原子半径逐渐减小,金属性逐渐减弱,对应的最高价氧化物的水化物的碱性逐渐减弱,非金属性逐渐增强,对应的最高价氧化物的水化物的酸性逐渐增强,以此解答该题.
解答:解:A.同周期元素从左到右元素的原子半径逐渐减小,原子序数逐渐增大,由原子半径大小关系可知原子序数W>Z>X,故A正确;
B.同一周期元素的原子半径越大,原子序数越小,非金属性越弱,对应的氢化物越不稳定,则气态氢化物的稳定性:N<R,故B错误;
C.图中元素应为第三周期元素,Y为金属Mg,W为非金属S,二者形成的化合物为离子化合物,故C错误;
D.Y为Na,Z为Al,对应的最高价氧化物的水化物分别为氢氧化钠和氢氧化铝,氢氧化铝具有两性,可与强碱反应,故D正确.
故选AD.
B.同一周期元素的原子半径越大,原子序数越小,非金属性越弱,对应的氢化物越不稳定,则气态氢化物的稳定性:N<R,故B错误;
C.图中元素应为第三周期元素,Y为金属Mg,W为非金属S,二者形成的化合物为离子化合物,故C错误;
D.Y为Na,Z为Al,对应的最高价氧化物的水化物分别为氢氧化钠和氢氧化铝,氢氧化铝具有两性,可与强碱反应,故D正确.
故选AD.
点评:本题考查同周期元素的性质的递变规律,侧重于学生的分析能力和基本概念的理解和运用的考查,为高频考点,注意把握同周期元素的性质的递变规律,难度不大.

练习册系列答案
相关题目
 (1)多电子原子核外电子能量是不同的,其中能层序数(n)越小,该能层能量
(1)多电子原子核外电子能量是不同的,其中能层序数(n)越小,该能层能量