题目内容
19.下列反应属于氧化还原反应的是①③⑥⑦,属于化合反应的是③⑤,属于分解反应的是②④,属于置换反应的是①,属于复分解反应的是⑧.①TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$2MgCl2+Ti
②CaCO3$\frac{\underline{\;煅烧\;}}{\;}$CaO+CO2↑
③2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3
④2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑
⑤H2O+SO3═H2SO4
⑥2Na2O2+2H2O═4NaOH+O2↑
⑦3NO2+H2O═2HNO3+NO
⑧NaOH+HCl═NaCl+H2O.
分析 含元素化合物变化的反应为氧化还原反应;
一种物质分解生成多种物质的反应为分解反应;
多种物质反应生成一种物质的反应为化合反应;
单质与化合物反应生成单质、化合物的反应为置换反应;
化合物与化合物反应生成两种新化合物的反应为复分解反应,以此来解答.
解答 解:①TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$2MgCl2+Ti为置换反应,Ti、Mg元素的化合价变化,为氧化还原反应;
②CaCO3$\frac{\underline{\;煅烧\;}}{\;}$CaO+CO2↑为分解反应,没有元素的化合价变化,不是氧化还原反应;
③2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3为化合反应,Fe、Cl元素的化合价变化,为氧化还原反应;
④2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑为分解反应,O元素的化合价变化,为氧化还原反应;
⑤H2O+SO3═H2SO4为化合反应,没有元素的化合价变化,不是氧化还原反应;
⑥2Na2O2+2H2O═4NaOH+O2↑不属于四种基本反应类型,过氧化钠中O元素的化合价变化,为氧化还原反应;
⑦3NO2+H2O═2HNO3+NO中N元素的化合价变化,为氧化还原反应;
⑧NaOH+HCl═NaCl+H2O为复分解反应,没有元素的化合价变化,为非氧化还原反应;
则属于氧化还原反应的是①③⑥⑦,属于化合反应的是③⑤,属于分解反应的是②④,属于置换反应的是①,属于复分解反应的是⑧,
故答案为:①③⑥⑦;③⑤;②④;①;⑧.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及与四种基本反应类型的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

| A. | 勒夏特列原理不能用于判断反应是否达平衡状态 | |
| B. | 浓度、压强、催化剂、温度等均能改变活化分子的百分数 | |
| C. | 能自发进行的反应其速率都很大 | |
| D. | 已知2C(s)+2O2(g)=2CO2(g)△H1,2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
①H2 ②CO ③CO和H2 ④HCOOCH3 ⑤HOOC-COOH ⑥C6H12O6 ⑦C12H22O11.
| A. | 全部 | B. | 仅④⑤ | C. | 仅①②③ | D. | 除⑤⑦外 |
①MgCl2 ②NaHCO3 ③(NH4)2S ④Al(OH)3.
| A. | 只有④ | B. | 除①外 | C. | 除①③ | D. | 全部都可以 |
| A. | 取出的10mL溶液中硝酸铜的物质的量浓度是1.6mol•L-1 | |
| B. | 取出的10mL溶液中Cu2+的物质的量浓度是0.16mol•L-1 | |
| C. | 取出的10mL溶液中硝酸铜的物质的量浓度是0.8mol•L-1 | |
| D. | 取出的10mL溶液中NO3-的物质的量浓度是1.6mol•L-1 |
①X+H2O→W+H2
②Y+H2O→N+O2
下列说法正确的是( )
| A. | X一定是非金属单质 | B. | X一定是金属单质 | ||
| C. | Y一定是非金属单质 | D. | Y一定是金属单质 |
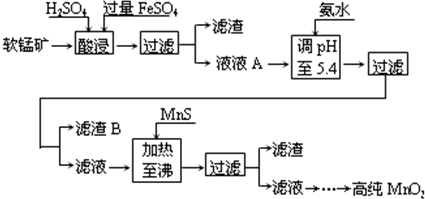
某软锰矿的主要成分为MnO2,还含有Si(16.72%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(2)滤渣B的主要成分有Fe(OH)3和Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.