题目内容
【题目】下列说法正确的是
A.1molH2的质量只有在标准状况下才约为2g
B.标准状况下,22.4L氖气含有的原子数为2NA
C.标准状况下,22.4LH2O含有的分子数为NA
D.同温同压下,相同体积的气体单质含有的原子数目不一定相等
【答案】D
【解析】
试题分析:A.1molH2的质量在任何条件下都约为2g,A错误;B.稀有气体是一个原子组成的,标准状况下,22.4L氖气含有的原子数为NA,B错误;C.标准状况下H2O不是气态,不能用摩尔体积计算含有的分子数,C错误;D.同温同压下,相同体积的气体单质含有的原子数目不一定相等,例如氧气和臭氧等,D正确,答案选D。

【题目】铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。
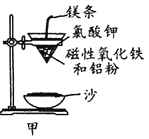
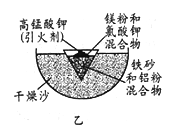
(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观。指明使用镁条和氯酸钾的目的是 ______________________。
(2)某同学用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色。为测定该实验所得 “铁块”中铁元素含量,设计实验流程如图所示。
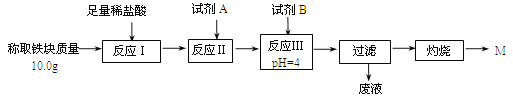
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
Fe2+ | Fe3+ | Al3+ | Mg2+ | |
开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
① 试剂A应选择________,试剂B应选择_______。(填序号)
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
② 写出反应Ⅱ的离子方程式_____________________。
③ 设计简单实验证明M的成分是Fe2O3而非Fe3O4。
操作 | 预期现象 |
取少量M固体于试管中,向其中加入________________;观察。 | 固体完全溶解,溶液呈黄色。 |
继续向上述溶液中滴入_________________,振荡观察 | ______________________ |
④ 上述实验应灼烧至M质量不变,则能证明M质量不变的标志是____________。
⑤ 若最终红色粉未M的质量为12.0 g,则该“铁块”的纯度是_______。