题目内容
8.用物质的量都是0.1mol的CH3COOH和CH3COONa配制成1L混合溶液,已知其中c(CH3COO-)大于c(Na+),则( )| A. | c(H+)<c(OH-) | B. | c(CH3COO-)=0.1mol/L-1 | ||
| C. | c(CH3COOH)<c(CH3COO-) | D. | c(CH3COO-)+c(OH-)=0.1mol/L-1 |
分析 CH3COOH和CH3COONa的混合溶液中只有4种离子,据电荷守恒有c(Na+)+c(H+)=c(CH3COO-)+c(OH-),c(CH3COO-)大于c(Na+),则c(H+)>c(OH-),说明溶液显酸性,醋酸根离子的水解程度小于醋酸的电离程度,c(Na+)=0.1mol/L-1,据此分析.
解答 解:A.CH3COOH和CH3COONa混合溶液中,存在c(Na+)+c(H+)=c(CH3COO-)+c(OH-),已知c(CH3COO-)>c(Na+),则c(H+)>C(OH-),故A错误;
B.c(Na+)=0.1mol/L,c(CH3COO-)大于c(Na+),故B错误;
C.CH3COOH和CH3COONa混合溶液,CH3COOH电离程度大于CH3COO-水解程度,则c(CH3COO-)>c(CH3COOH),故C正确;
D.CH3COOH和CH3COONa混合溶液中,存在c(Na+)+c(H+)=c(CH3COO-)+c(OH-),醋酸为弱电解质,存在微弱电离,则有0.1mol/L>c(CH3COOH)>c(H+),c(Na+)=0.1mol/L,则0.1mol/L-1<c(CH3COO-)+c(OH-)<0.2mol•L-1,故D错误;
故选C.
点评 本题考查弱电解质和盐类水解问题,题目难度中等,注意根据溶液电中性和物料守恒解答该题.

练习册系列答案
相关题目
18.下列说法不正确的是( )
| A. | 过氧化钠、烧碱、纯碱分别属于碱性氧化物、碱、盐 | |
| B. | 乙醇和水可以任意比互溶,主要是因为乙醇和水分子间能形成氢键 | |
| C. | 硫酸钡、冰醋酸、酒精分别属于强电解质、弱电解质、非电解质 | |
| D. | 煤的气化、液化和干馏均属于化学变化 |
19.下列有关氧族元素的叙述中,正确的是( )
| A. | 都能生成+6价化合物 | B. | 原子的最外层电子数都是6 | ||
| C. | 都能生成稳定的氢化物 | D. | 单质在通常情况下均为固体 |
16.下列说法正确的是( )
| A. | 0.2mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-) | |
| B. | 向NH4Cl溶液中加入少量氨水,当pH=7时,则混合液中:c(NH4+)=c(Cl-) | |
| C. | 0.1mol•L-1的Na2S溶液中:c(Na+)=2c(S2-) | |
| D. | 某溶液的pH为6,则该溶液一定显酸性 |
13.下列哪组离子能在水溶液中大量共存( )
| A. | K+、CO32-、HS-、S2-、Al3+、AlO2- | B. | MnO4-、Na+、SO42-、Fe3+、NH4+ | ||
| C. | SO42-、Ag+、SO32-、S2-、AlO2-、K+ | D. | Fe2+、Cl-、H+、NO3- |
20.常温下,下列溶液的离子浓度关系式正确的是( )
| A. | pH=6的H2S溶液中,c(H+)=c(HS-)=1×10-6mol•L-1 | |
| B. | pH=a的醋酸溶液,稀释10倍后,其pH=b,则b=a+1 | |
| C. | pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,溶液pH<7:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | pH相同的①CH3COONa、②Na2CO3、③NaClO三种溶液的c(Na+):①<②<③ |
17.下列四组物质的质量相等,其中加热分解得到氨气的质量最大的是( )
| A. | 碳酸氢铵和氢氧化钠按物质的量1:1混合 | |
| B. | 硫酸铵和氢氧化钠按物质的量1:2混合 | |
| C. | 氯化铵和氢氧化钠按物质的量1:1混合 | |
| D. | 碳酸铵和氢氧化钠按物质的量1:2混合 |

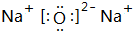 ,C的化学式Cl2.
,C的化学式Cl2.