��Ŀ����
��¯���������з�������Ҫ��ӦΪ��
Fe2O3��s��+CO��g��?
Fe��s��+CO2��g��
��֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�������
��ش��������⣺
��1���÷�Ӧ��ƽ�ⳣ������ʽK= ����H 0�����������������=������
��2����һ���ݻ�Ϊ10L���ܱ������У�1 000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol����Ӧ����10min��ﵽƽ�⣮���ʱ�䷶Χ�ڷ�Ӧ��ƽ�ⷴӦ����v��CO2��= ��CO��ƽ��ת����= ��
| 1 |
| 3 |
| 2 |
| 3 |
��֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�������
| �¶�/�� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
��1���÷�Ӧ��ƽ�ⳣ������ʽK=
��2����һ���ݻ�Ϊ10L���ܱ������У�1 000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol����Ӧ����10min��ﵽƽ�⣮���ʱ�䷶Χ�ڷ�Ӧ��ƽ�ⷴӦ����v��CO2��=
���㣺��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
��������1����ѧƽ�ⳣ������ָ��һ���¶��£����淴Ӧ�ﵽƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ���ݴ���д��ע����塢��Һ���Ũ��Ϊ����������Ҫд���塢��Һ�壻
�ɱ������ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС���������¶�ƽ�����淴Ӧ�ƶ�������ӦΪ���ȷ�Ӧ��
��2����ƽ��ʱCO�����ʵ����仯Ϊnmol����������ʽ��ʾ��ƽ��ʱCO��CO2�����ʵ�������ѧ����������1���������ʵ�������Ũ�ȴ���ƽ�ⳣ������n��ֵ����������CO��Ũ�ȱ仯��������v=
����v��CO����������ת���ʶ������CO��ת���ʣ�
�ɱ������ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС���������¶�ƽ�����淴Ӧ�ƶ�������ӦΪ���ȷ�Ӧ��
��2����ƽ��ʱCO�����ʵ����仯Ϊnmol����������ʽ��ʾ��ƽ��ʱCO��CO2�����ʵ�������ѧ����������1���������ʵ�������Ũ�ȴ���ƽ�ⳣ������n��ֵ����������CO��Ũ�ȱ仯��������v=
| ��c |
| ��t |
���
�⣺��1����Ӧ
Fe2O3��s��+CO��g��?
Fe��s��+CO2��g����ƽ�ⳣ��k=
��
�ɱ������ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС���������¶�ƽ�����淴Ӧ�ƶ�������ӦΪ���ȷ�Ӧ������H��0��
�ʴ�Ϊ��
������
��2����ƽ��ʱCO�����ʵ����仯Ϊnmol����
Fe2O3��s��+CO��g��?
Fe��s��+CO2��g��
��ʼ��mol����1 1
�仯��mol����n n
ƽ�⣨mol����1-n n+1
����
=4�����n=0.6��
����v��CO2��=
mol?L-1?min-1=0.006 mol?L-1?min-1��
CO��ƽ��ת����Ϊ
��100%=60%��
�ʴ�Ϊ��0.006 mol?L-1?min-1��60%��
| 1 |
| 3 |

| 2 |
| 3 |
| c(CO2) |
| c(CO) |
�ɱ������ݿ�֪���¶�Խ��ƽ�ⳣ��ԽС���������¶�ƽ�����淴Ӧ�ƶ�������ӦΪ���ȷ�Ӧ������H��0��
�ʴ�Ϊ��
| c(CO2) |
| c(CO) |
��2����ƽ��ʱCO�����ʵ����仯Ϊnmol����
| 1 |
| 3 |

| 2 |
| 3 |
��ʼ��mol����1 1
�仯��mol����n n
ƽ�⣨mol����1-n n+1
����
| n+1 |
| 1-n |
����v��CO2��=
| ||
| 10 |
CO��ƽ��ת����Ϊ
| 0.6 |
| 1 |
�ʴ�Ϊ��0.006 mol?L-1?min-1��60%��
���������⿼�黯ѧƽ����йؼ��㡢��ѧ��Ӧ���ʼ��㡢ƽ�ⳣ���ȣ��Ѷ��еȣ�ע�����ջ�ѧƽ�ⳣ����Ӧ�ã�1�������жϷ�Ӧ���еij̶ȣ�2���жϷ�Ӧ����ЧӦ��3���жϷ�Ӧ���еķ���4�������������ʵ�ת���ʣ�

��ϰ��ϵ�д�
�����Ŀ
���й����л����˵����ȷ���ǣ�������
| A����ֻ�ܷ���ȡ����Ӧ�����ܷ���������Ӧ�ͼӳɷ�Ӧ |
| B�����ۡ���֬�������ʾ����ڸ߷��ӻ����ˮ����������ͬ |
| C���ױ�����ʹ���Ը��������Һ��ɫ |
| D����ȥ�Ҵ�������������ɼ���������ʯ�ң�Ȼ������ |
Ǧ���ص������ֱ���Pb��PbO2���������ҺΪ30%���ᣬ����ʱ��ӦΪ��Pb+PbO2+2H2SO4
2PbSO4+2H2O����ŵ�ʱ�����н�����ȷ���ǣ�������
| �ŵ� |
| ��� |
| A��PbO2������������ |
| B����ص������Һ���ܶȲ��ϼ�С |
| C��c��H+�������� |
| D��H+���ƶ� |
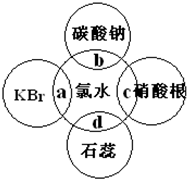
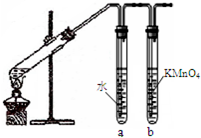 Ϊ�������������鷢����ȥ��Ӧ�����ɵ��������Ƿ���ϩ��װ����ͼ��ʾ���ش�
Ϊ�������������鷢����ȥ��Ӧ�����ɵ��������Ƿ���ϩ��װ����ͼ��ʾ���ش�