题目内容
13.A、CH4、H2组成的混合气体,当V(A):V(H2)=7:24时混合气体的摩尔质量为16g•mol-1则A为( )| A. | O2 | B. | CO | C. | CO2 | D. | SO2 |
分析 当V(A):V(H2)=7:24时,混合气体的摩尔质量为16g•mol-1,由于CH4的摩尔质量也为16g/mol,故甲烷的量对混合物气体的平均摩尔质量无影响.
设A的摩尔质量为xg/mol,则有:$\overline{M}$=16g/mol=$\frac{xg/mol×7mol+2g/mol×24mol}{7mol+24mol}$,据此分析.
解答 解:当V(A):V(H2)=7:24时,混合气体的摩尔质量为16g•mol-1,由于CH4的摩尔质量也为16g/mol,故甲烷的量对混合物气体的平均摩尔质量无影响.
设A的摩尔质量为xg/mol,由于气体的体积之比等于物质的量之比,故设A的物质的量为7mol,氢气的物质的量为24mol,则混合物气体的平均摩尔质量有:$\overline{M}$=16g/mol=$\frac{xg/mol×7mol+2g/mol×24mol}{7mol+24mol}$,解得X=64g/mol,故选D.
点评 本题考查了混合物气体中的组分气体的摩尔质量的求算,应注意其组分之一甲烷的摩尔质量也为16g/mol,对混合物的摩尔质量无影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.类推是化学中常用的思维方法,以下四个类推结果正确的是( )
| A. | 氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物 | |
| B. | 酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸和碱的反应 | |
| C. | 燃烧一般都伴随着发光,发热现象,所以有发光.发热的现象就是燃烧 | |
| D. | 醇类物质在空气中燃烧生成CO2 和H2O,甲醇是醇类的一种,所以甲醇在空气中燃烧生成CO2 和H2O |
4.为了除去粗盐中Ca2+、Mg2+、SO${\;}_{4}^{2-}$及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液.其中正确的操作顺序是( )
| A. | ④②⑤①③ | B. | ②④⑤①③ | C. | ④⑤②①③ | D. | ⑤②④①③ |
8.对危险化学品要在包装标签上印上警示性标志.下列的化学药品名称与警示标志名称对应不正确的是( )
| A. | 酒精--易燃品 | B. | 浓硫酸--腐蚀品 | ||
| C. | 烧碱--剧毒品 | D. | 氯酸钾--强氧化剂 |
18.在乙醇CH3CH2OH中化学键如图,则下列说法中正确的是( )
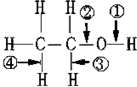

| A. | 当该醇发生催化氧化时,被破坏的键是②③ | |
| B. | 当该醇与Na反应时,被破坏的键是① | |
| C. | 当该醇与羧酸发生酯化反应时,被破坏的键是② | |
| D. | 当该醇发生消去反应时,被破坏的键是①和④ |
2.同温同压下,下列几种气体中,等质量时所占体积最大的是( )
| A. | CO | B. | H2 | C. | CO2 | D. | Cl2 |

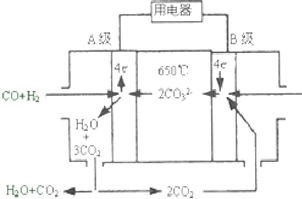 熔融碳酸盐燃料电池(MCFS),发明于1889年.现有一个碳酸盐燃料电池,以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示.请回答下列问题:
熔融碳酸盐燃料电池(MCFS),发明于1889年.现有一个碳酸盐燃料电池,以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示.请回答下列问题: