题目内容
【题目】二氧化氯(ClO2)广泛应用于纸浆漂白、杀菌消毒和水净化处理等领域。工业上利用甲醇还原NaClO3的方法制备ClO2,工艺流程如下:
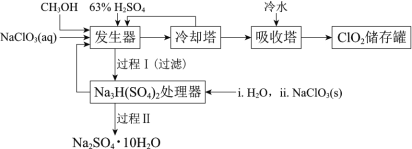
已知:a.发生器中制备ClO2的反应:12NaClO3+8H2SO4+3CH3OH=12ClO2↑+3HCOOH+4Na3H(SO4)2↓+9H2Ob.相关物质的熔沸点:

(1)ClO2可用于纸浆漂白、杀菌消毒是因其具有_____性。
(2)冷却塔用于分离ClO2并回收CH3OH,应控制的最佳温度为 ______________(填字母)。
a.0~10℃ b.20~30℃ c.60~70℃
(3)可以获得芒硝(Na2SO4·10H2O)并使部分原料循环利用。已知:Na2SO4·10H2O和Na2SO4的溶解度曲线如图:

① Na3H(SO4)2处理器中获得芒硝时需加入NaClO3固体,从芒硝溶解平衡的角度解释其原因 __(结合方程回答)。
②结合Na2SO4·10H2O和Na2SO4的溶解度曲线,过程Ⅱ的操作是:在32.4℃恒温蒸发,_______。
③Na3H(SO4)2处理器的滤液中可以循环利用的原料是NaClO3和_____。
(4)为测定存储罐中所得溶液中ClO2的含量,进行了以下实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100 mL试样。
步骤2:量取V1mL试样加入到锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇 匀,在暗处静置30分钟。(已知:ClO2+I-+H+—I2+Cl-+H2O 未配平)
步骤3:以淀粉溶液作指示剂,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。(已知:I2+2S2O32-=2I-+S4O62-)
①准确量取10.00 mL ClO2溶液的玻璃仪器是______。
②若实验中使用的Na2S2O3标准溶液部分因被氧气氧化而变质,则实验结果_____ (填“偏高”、“偏低”或“无影响”)
③根据上述步骤可计算出原ClO2溶液的浓度为_____mol·L-1(用含字母的代数式表示)。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。ClO2的有效氯含量为_______。(计算结果保留两位小数)
【答案】氧化 B Na2SO410H2O(s)2Na+(aq)+SO42-(aq)+10H2O(l),加入NaClO3使溶液中c(Na+)增大,平衡逆向移动,使Na2SO410H2O晶体析出 冷却结晶、过滤、洗涤、干燥 H2SO4 酸式滴定管 偏高 ![]() 2.63g
2.63g
【解析】
发生器中发生反应:12NaClO3+8H2SO4+3CH3OH═12ClO2↑+3HCOOH+4Na3H(SO4)2↓+9H2O,过滤得到不溶性Na3H(SO4)2滤渣和含有CH3OH等物质的滤液,滤液在冷却塔中冷却分离出ClO2气体,含有CH3OH等物质的滤液循环到发发生器中,充分利用原料CH3OH和NaClO3,ClO2气体在吸收塔中冰水冷却至液体ClO2储存;处理器中,Na3H(SO4)2滤渣在Na+作用下与水转化为Na2SO410H2O和H2SO4,过滤得到芒硝Na2SO410H2O,滤液中的H2SO4和NaClO3循环到发生器中充分利用,据此分析解答(1)~(3);
(4)ClO2溶液显酸性,结合2ClO2+10I-+8H+=2Cl-+5I2+4H2O、I2+2S2O32-═2I-+S4O62-得关系式ClO2~5S2O32-,据此计算原ClO2溶液的浓度;
(5)根据每克含氯消毒剂转移的电子,结合ClO2~Cl-~5e-,Cl2~2Cl-~2e-分析计算。
(1)ClO2具有强氧化性,可用于纸浆漂白、杀菌消毒,故答案为:氧化;
(2)ClO2的沸点为11℃,CH3OH沸点为65℃,便于分离气态的ClO2和液态的含有CH3OH的滤液,冷却塔中控制的温度在11~65℃之间,结合后续实验的冷却,则最佳温度应该控制在20~30℃,故答案为:B;
(3)①Na2SO410H2O晶体在溶液中存在溶解和结晶的平衡,即Na2SO410H2O(s)2Na+(aq)+SO42-(aq)+10H2O(l),根据平衡移动原理可知,加入NaClO3使溶液中c(Na+)增大,平衡逆向移动,使Na2SO410H2O晶体析出,故答案为:Na2SO410H2O(s)2Na+(aq)+SO42-(aq)+10H2O(l),加入NaClO3使溶液中c(Na+)增大,平衡逆向移动,使Na2SO410H2O晶体析出;
②由Na2SO410H2O和Na2SO4的溶解度曲线可知,32.4℃时Na2SO410H2O和Na2SO4的溶解度均处于最大,但Na2SO410H2O的溶解度随温度的升高而增大,Na2SO4的溶解度随温度的升高而较小,防止Na2SO4结晶析出,应采用降温结晶法得到Na2SO410H2O,即恒温蒸发浓缩溶液、冷却结晶、过滤、洗涤、干燥,故答案为:冷却结晶、过滤、洗涤、干燥;
③在Na+作用下,Na3H(SO4)2滤渣在处理器中与水转化为Na2SO410H2O和H2SO4,过滤得到芒硝Na2SO410H2O,滤液中的H2SO4和NaClO3循环到发发生器中充分利用,故答案为:H2SO4。
(4)①ClO2溶液显酸性,所以准确量取10.00 mL ClO2溶液的玻璃仪器是酸式滴定管,故答案为:酸式滴定管;
②Na2S2O3标准溶液部分因被氧气氧化而变质,则消耗的Na2S2O3标准溶液体积偏大,根据I2+2S2O32-=2I-+S4O62-,2ClO2+10I-+8H+=2Cl-+5I2+4H2O可知,测得的ClO2偏多,导致测定结果偏高,故答案为:偏高;
③由方程式2ClO2+10I-+8H+=2Cl-+5I2+4H2O、I2+2S2O32-═2I-+S4O62-得关系式ClO2~5S2O32-,n(S2O32-)=cV2×10-3mol,所以V1mL ClO2的溶液中含有的ClO2的物质的量为2cV2×10-4mol,则10mL的原溶液含有ClO2的物质的量为:2cV2×10-4mol×![]() =
=![]() ×10-2mol,所以原ClO2溶液的物质的量浓度为
×10-2mol,所以原ClO2溶液的物质的量浓度为 =
=![]() mol/L,故答案为:
mol/L,故答案为:![]() ;
;
(5)根据有效氯定义,1gC1O2的物质的量为![]() mol,依据电子转移数目相等,ClO2~Cl-~5e-,Cl2~2Cl-~2e-,则转移电子为
mol,依据电子转移数目相等,ClO2~Cl-~5e-,Cl2~2Cl-~2e-,则转移电子为![]() mol,可知氯气的物质的量为
mol,可知氯气的物质的量为![]() ×
×![]() mol,则氯气的质量为
mol,则氯气的质量为![]() ×
×![]() mol×71g/mol=2.63g,故答案为:2.63g。
mol×71g/mol=2.63g,故答案为:2.63g。








