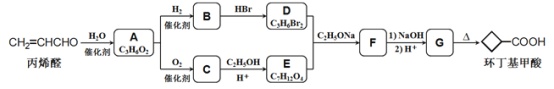
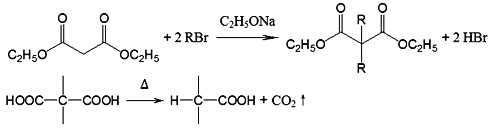
题目内容
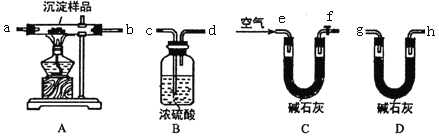
【题目】(1)工业上用洗净的废铜屑作原料来制备硫酸铜。下列制备方法符合“绿色化学”思想的是_________(填序号)。
①![]() ②
②![]()
写出①中反应的化学方程式:_____________________。
(2)SO2被称为“空中死神”,其对环境的危害常表现为__________________。为了减少危害,人们进行了许多有益的探索和研究,并且在实际应用上取得了一定的成果。工业上常用生石灰来处理煤炭中的SO2,这是利用了SO2属于__________氧化物的性质。
(3)硫元素是一种常见的非金属元素,硫原子的原子结构示意图为_______,自然界中存在的某种单质以八个原子结合,其分子式为_______。
(4)氮元素是大气中含量最高的元素,其单质的电子式___________。由于该单质比较稳定,只能与部分活泼金属反应,比如在点燃条件下,可与金属镁反应,试写出该反应方程式___________________________。
【答案】 ② Cu + 2H2SO4(浓)![]() CuSO4 + SO2 ↑ + 2H2O 形成酸雨 酸性
CuSO4 + SO2 ↑ + 2H2O 形成酸雨 酸性 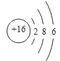 S8
S8 ![]() 3Mg+N2
3Mg+N2![]() Mg3N2
Mg3N2
【解析】(1)原子利用率达到100%符合绿色化学;铜与浓硫酸反应生成硫酸铜、二氧化硫和水;
(2)根据二氧化硫的性质以及对环境的危害分析解答;
(3)硫原子的质子数是16,据此书写结构示意图;根据硫原子的个数书写分子式;
(4)氮气分子中含有三键;氮气与镁反应生成氮化镁。
(1)铜与浓硫酸反应生成硫酸铜、二氧化硫和水,有污染性气体二氧化硫生成,原子利用率不是100%,因此符合“绿色化学”思想的是反应②。铜与浓硫酸反应生成硫酸铜、二氧化硫和水,反应的化学方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
(2)SO2被称为“空中死神”,其对环境的危害常表现为形成酸雨。二氧化硫是酸性氧化物,能与碱性氧化物氧化钙反应,因此工业上常用生石灰来处理煤炭中的SO2。
(3)硫原子的原子序数是16,原子结构示意图为 ;自然界中存在的某种单质以八个原子结合,其分子式为S8。
;自然界中存在的某种单质以八个原子结合,其分子式为S8。
(4)氮元素是大气中含量最高的元素,其单质的电子式为![]() 。在点燃条件下,氮气可与金属镁反应生成氮化镁,该反应的方程式为3Mg+N2
。在点燃条件下,氮气可与金属镁反应生成氮化镁,该反应的方程式为3Mg+N2![]() Mg3N2。
Mg3N2。

 名校课堂系列答案
名校课堂系列答案