题目内容
【题目】工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
探究一
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________。
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中的Fe2+,应选用_______选填序号)
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c..浓氨水 d.酸性KMnO4溶液
②乙同学取336mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为____________。
探究二
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含少量的H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
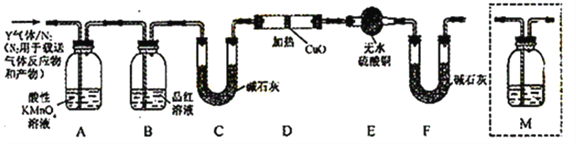
(3)装置B中试剂的作用是___________。
(4)认为气体Y中还含有Q的理由是___________(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于____________(选填序号)。
a. A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是___________。
【答案】 其原因是铁钉表面被钝化(或其它合理答案)。 应选用 d 选填序号)。 SO2的体积分数为66.7%(或其它合理答案)。 装置B中试剂的作用是检验SO2是否除尽。 理由是C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。 添加M于 c (选填序号)。 预计实验现象应是D中固体由黑变红和E中固体由白变蓝。
CO2↑+2SO2↑+2H2O。 添加M于 c (选填序号)。 预计实验现象应是D中固体由黑变红和E中固体由白变蓝。
【解析】试题分析:(1)铁钉放入冷硫酸中,浓硫酸有较强的氧化性能使铁钉钝化阻止反应进一步进行。
(2)①亚铁离子能使酸性高锰酸钾褪色,溶液中已经有三价铁离子,选择a会造成干扰;b能检验三价铁离子的存在;选c生成两种沉淀,受氢氧化铁沉淀颜色的影响无法分辨;Fe2+与酸性KMnO4溶液发生氧化还原反应,Fe2+能使酸性KMnO4溶液褪色,故选d; SO2具有还原性,通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4,生成的硫酸遇到氯化钡会产生白色沉淀,则n(混合气体)=0.336L÷22.4L/mol=0.015mol,根据对应关系:SO2~ BaSO4,
n(SO2)=n(BaSO4)=2.33g÷233g/mol,解得n(SO2)=0.01mol,所以二氧化硫的体积分数为:0.01mol÷0.015mol×100%=66.7%。
(3)A除去二氧化硫,二氧化硫能使品红溶液褪色,所以B可以检验A中是否完全除去二氧化硫。
(4)在加热时,铁钉中不仅铁和浓硫酸反应,碳也和浓硫酸反应生成生成二氧化硫、二氧化碳和水,反应方程式为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(5)Q为二氧化碳,二氧化碳和二氧化硫都能使澄清石灰水变浑浊,选择a或b受二氧化硫的影响无法判断二氧化碳的存在,选d时二氧化碳被碱石灰吸收,B-C间加入澄清石灰水可检验CO2,故选c。
(6)氢气还原氧化铜会生成水蒸气能使白色的硫酸铜粉末变蓝色,同时有红色的铜单质生成,故答案为:D中固体由黑色变红和E中固体由白变蓝。