题目内容
【题目】I.NO是第一个被发现的生命体系气体信号分子,具有舒张血管的功能。工业上可用“氨催化氧化法”生产NO,主要副产物为N2。请回答下列问题:
(1)以氨气、氧气为原料,在催化剂存在下生成NO和副产物N2的热化学方程式如下:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H1①,4NH3(g)+3O2(g)
4NO(g)+6H2O(g) △H1①,4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) △H2②,N2(g)+O2(g)
2N2(g)+6H2O(g) △H2②,N2(g)+O2(g)![]() 2NO(g) △H3③,则上述反应热效应之间的关系式为△H3 =___________________。
2NO(g) △H3③,则上述反应热效应之间的关系式为△H3 =___________________。
(2)某化学研究性学习小组模拟工业合成NO的反应。在1110K时,向一恒容密闭容器内充入1mol NH3和2.8mol O2,加入合适催化剂(催化剂的体积大小可忽略不计),保持温度不变,只发生反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H<0。
4NO(g)+6H2O(g) △H<0。
①下列各项能说明反应已达到化学平衡状态的是_______。(填字母序号)
a.5c(NH3)=4c(O2)
b.N-H键的生成速率与O-H键的生成速率相等
c.混合气体的压强不变
d.混合气体的密度不变
②若其他条件不变,将容器改为恒容的绝热容器,在达到平衡后的体系温度下的化学平衡常数为K1,则K1_____K(填“>”、“<”或“=”)。
II.(3)某化学研究性学习小组模拟用CO和H2合成甲醇,其反应为:CO(g)+2H2(g) ![]() CH3OH(g)△H<O。在容积固定为1L的密闭容器内充入2mol CO和4 mol H2,加入合适的催化剂(体积可以忽略不计)、保持250℃不变发生上述反应,用压力计监测容器内压强的变化如下:
CH3OH(g)△H<O。在容积固定为1L的密闭容器内充入2mol CO和4 mol H2,加入合适的催化剂(体积可以忽略不计)、保持250℃不变发生上述反应,用压力计监测容器内压强的变化如下:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
压强/MPa | 12.4 | 10.2 | 8.4 | 7.0 | 6.2 | 6.2 |
则反应从开始到20min时,以CO浓度变化表示的平均反应速率v(CO)=_______,该温度下平衡常数K=_______。
III.(4)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
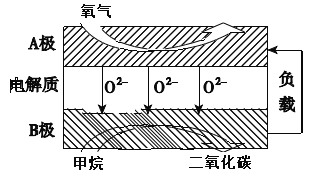
①B极上的电极反应式为_____________。
②若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到5.6 L(标准状况)气体时,消耗甲烷的体积为________L(标准状况下)。
【答案】 △H3=(△H1—△H2 )/2 b c < 0. 075 mol/(L﹒min) 3(mol/L)-2 (单位不作要求) CH4-8e-+4O2-=CO2+2H2O 2.8
【解析】
(1)由盖斯定律计算可得△H3;
(2)①根据化学平衡状态的特征分析,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、质量、体积分数以及百分含量不变,以及由此衍生的一些量也不发生变化,注意选择的物理量应随反应进行发生变化,该物理量由变化到不变,说明到达平衡;
②该反应为放热反应,反应过程中反应温度升高,平衡向逆反应方向移动,化学平衡常数减小;
(3)依据表给数据建立三段式,通过化学反应速率公式和化学平衡常数公式计算化学反应速率和化学平衡常数;
(4)①由阴离子移动方向可知B为负极,负极发生氧化反应,甲烷被氧化生成二氧化碳和水;
②依据得失电子数目守恒计算消耗甲烷的体积。
(1)由盖斯定律可知,(①—②)/2得N2(g)+O2(g)![]() 2NO(g),则△H3=(△H1—△H2 )/2,故答案为:△H3=(△H1—△H2 )/2;
2NO(g),则△H3=(△H1—△H2 )/2,故答案为:△H3=(△H1—△H2 )/2;
(2)①a、5c(NH3)=4c(O2)与反应的初始物质的量以及反应的转化程度有关,不能确定是否达到平衡,错误;
b、N-H键的生成速率与O-H键的生成速率相等说明正逆反应速率相等,反应达到平衡状态,正确;
c、该反应是一个反应前后气体体积改变的化学反应,当反应达到平衡状态时,各物质的量不变,导致容器中压强不随时间的变化而改变,混合气体的压强不变能够说明反应达到平衡状态,正确;
d、容器是恒容的,无论反应是否达到平衡状态,混合物的质量始终不变,容器的体积不变,导致密度始终不变,混合气体的密度不变不能说明费用达到平衡,错误;
故选bc,故答案为:bc;
②该反应为放热反应,若其他条件不变,将容器改为恒容的绝热容器,反应过程中反应温度升高,平衡向逆反应方向移动,化学平衡常数减小,故答案为:<;
(3)由表中数据可知,20min时处于平衡状态,设CO的转化率为x,依据题意建立如下三段式:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始量(mol):2 4 0
变化量(mol):x 2x x
平衡量(mol):2-x 4-2x x
压强之比等于物质的量之比,则平衡时混合气体总物质的量为(2mol+4mol)×6.2MPa/12.4MPa=(6-2x)mol,解得x=1.5 mol,则反应消耗c(CO)=1.5mol/1L=1.5 mol/L,
以CO浓度变化表示的平均反应速率v(CO)=1.5 mol/L/20min=0.075mol/(L.min);化学平衡常数K=c(CH3OH)/c(CO)c2(H2)= 1.5 mol/L/0.5 mol/L×(1 mol/L)2=3(mol/L)-2,故答案为:0.075mol/(L.min);3(mol/L)-2;
(4)①由阴离子移动方向可知B为负极,负极发生氧化反应,甲烷被氧化生成二氧化碳和水,电极方程式为CH4+4O2--8e-=CO2+2H2O,故答案为:CH4+4O2--8e-=CO2+2H2O;
②若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到5.6L(标准状况)氧气时,反应转移1mol 电子,由得失电子数目守恒可知消耗甲烷的物质的量为0.125mol,则甲烷的体积为0.125mol×22.4mol/L=2.8L,故答案为:2.8。

 53天天练系列答案
53天天练系列答案