题目内容
【题目】根据下表回答问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ⑤ | |||||
3 | ③ | ⑥ | |||||
4 | ④ | ⑦ | |||||
(1)表中______(填元素符号)的非金属性最强;______(填元素符号)的金属性最强,写出该元素的单质与水反应的离子方程式:______。
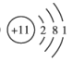
(2)表中元素③的原子结构示意图是______。
(3)表中元素⑤、⑦的氢化物的稳定性顺序为______>______(填化学式)。
(4)表中元素最高价氧化对应水化物中酸性最强的是______(填化学式)。
【答案】F K 
![]()
![]()
![]()
【解析】
根据元素在周期表中的相对位置可知,①~⑦分别是H元素、Li元素、Na元素、K元素、F元素、Cl元素、Br元素。
(1)由元素周期律可知,非金属性最强的元素位于元素周期表右上角(稀有气体除外),金属性最强的元素位于元素周期表左下角,则F元素的非金属性最强,K的金属性最强,钾与水反应生成氢氧化钾和氢气,反应的离子方程式为2K+2H2O=2K++2OH-+H2↑,故答案为:F;K;2K+2H2O=2K++2OH-+H2↑;
(2)钠原子核外有11个电子,3个电子层,最外层有1个电子,原子结构示意图为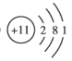 ,故答案为:
,故答案为: ;
;
(3)元素的非金属性越强,氢化物的稳定性越强,同主族的F元素非金属性强于Br元素,则氢化物的稳定性HF强于HBr,故答案为:HF;HBr;
(4)元素的非金属性越强,最高价氧化物对应水化物的酸性越强,氟元素没有正化合价,没有含氧酸,则表中元素最高价氧化物对应水化物中酸性最强的是HClO4,故答案为:HClO4。

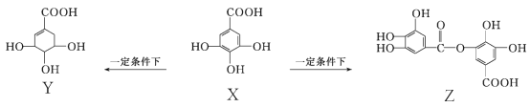
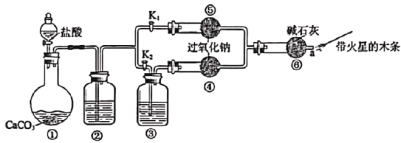
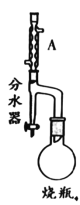
【题目】实验室制备甲基丙烯酸甲酯的反应装置示意图和有关信息如下:
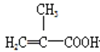 +CH3OH
+CH3OH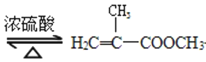 +H2O
+H2O
药品 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度(gcm-3) |
甲醇 | 32 | -98 | -64.5 | 与水混溶,易溶于有机溶剂 | 0.79 |
甲基丙烯酸 | 86 | 15 | 161 | 溶于热水,易溶于有机剂 | 1.01 |
甲基丙烯酸甲酯 | 100 | -48 | 100 | 微溶于水,易溶于有机溶剂 | 0.944 |
已知甲基丙烯酸甲酯受热易聚合;甲基丙烯酸甲酯在盐溶液中溶解度较小;CaCl2可与醇结合形成复合物;
实验步骤:
①向100mL烧瓶中依次加入:15mL甲基丙烯酸、2粒沸石、10mL无水甲醇、适量的浓硫酸;
②在分水器中预先加入水,使水面略低于分水器的支管口,通入冷凝水,缓慢加热 烧瓶。在反应过程中,通过分水器下部的旋塞分出生成的水,保持分水器中水层液面的高度不变,使油层尽量回到圆底烧瓶中;
③当 ,停止加热;
④冷却后用试剂 X 洗涤烧瓶中的混合溶液并分离;
⑤取有机层混合液蒸馏,得到较纯净的甲基丙烯酸甲酯。请回答下列问题:
(1)A装置的名称是_____。
(2)请将步骤③填完整____。
(3)上述实验可能生成的副产物结构简式为_____(填两种)。
(4)下列说法正确的是______
A.在该实验中,浓硫酸是催化剂和脱水剂
B.酯化反应中若生成的酯的密度比水大,不能用分水器提高反应物的转化率
C.洗涤剂X是一组试剂,产物要依次用饱和Na2CO3、饱和CaCl2溶液洗涤
D.为了提高蒸馏速度,最后一步蒸馏可采用减压蒸馏;该步骤一定不能用常压蒸馏
5)实验结束收集分水器分离出的水,并测得质量为2.70g,计算甲基丙烯酸甲酯的产率约为_____。实验中甲基丙烯酸甲酯的实际产率总是小于此计算值,其原因不可能是_____。
A.分水器收集的水里含甲基丙烯酸甲酯
B.实验条件下发生副反应
C.产品精制时收集部分低沸点物质
D.产品在洗涤、蒸发过程中有损失