题目内容
NA表示阿伏加德罗常数的值,则下列说法中不正确的是( )
| A、31g白磷中含有0.25NA个分子 |
| B、1mol铵根离子中含有的电子数为9NA |
| C、8克甲烷分子中所含共用电子对数为2NA |
| D、16g氧气和臭氧的混合物中含有NA个氧原子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.白磷的分子式为P4,摩尔质量为124g/mol,31g白磷中含有白磷分子的物质的量为0.25mol;
B.铵根离子中含有10个电子,1mol铵根离子含有10mol电子;
C.甲烷分子中含有4个碳氢共价键,8个甲烷的物质的量为0.5mol,含有2mol共用电子对;
D.臭氧和氧气中都只含有氧原子,16个二者的混合物中含有16个氧原子,含有1mol氧原子.
B.铵根离子中含有10个电子,1mol铵根离子含有10mol电子;
C.甲烷分子中含有4个碳氢共价键,8个甲烷的物质的量为0.5mol,含有2mol共用电子对;
D.臭氧和氧气中都只含有氧原子,16个二者的混合物中含有16个氧原子,含有1mol氧原子.
解答:
解:A.31g白磷中含有白磷分子的物质的量为:
=0.25mol,含有0.25NA个白磷分子,故A正确;
B.1mol铵根离子中含有10mol电子,含有的电子数为10NA,故B错误;
C.8g甲烷的物质的量为0.5mol,0.5mol甲烷分子中含有2mol共用电子对,所含共用电子对数为2NA,故C正确;
D.16g氧气和臭氧的混合物中含有16个氧原子,含有1mol氧原子,含有NA个氧原子,故D正确;
故选B.
| 31g |
| 124g/mol |
B.1mol铵根离子中含有10mol电子,含有的电子数为10NA,故B错误;
C.8g甲烷的物质的量为0.5mol,0.5mol甲烷分子中含有2mol共用电子对,所含共用电子对数为2NA,故C正确;
D.16g氧气和臭氧的混合物中含有16个氧原子,含有1mol氧原子,含有NA个氧原子,故D正确;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,选项A为易错点,注意白磷分子的组成情况.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )
| A、标准状况下,48g O3含有的氧原子数为3NA |
| B、1mol OH-离子中含电子数目为10NA |
| C、0.5L 0.2mol?L-1的NaCl溶液中含有的Na+数是0.1NA |
| D、常温常压下,33.6L CO中含有的原子数是3NA |
下列各组物质的性质比较,正确的是( )
| A、碱性:KOH>Ca(OH)2>NaOH |
| B、氢化物稳定性:NH3>H2O>HF |
| C、酸性:HClO>H2SO4>H3PO4 |
| D、氧化性:F2<Cl2<Br2<I2 |
下列物质的工业制备原理的方程式书写正确的是( )
| A、氢氧化钠:Na2CO3+Ca(OH)2→CaCO3↓+2NaOH | ||
B、乙醇:C6H12O6
| ||
C、二氧化硫:Cu+2H2SO4(浓)
| ||
D、氯气:Ca(ClO)2+4HCl(浓)
|
类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实践的验证.以下类推的结论正确的是( )
| A、不能用电解AlCl3来制取Al,也不能用电解MgCl2来制取镁 |
| B、金刚石的硬度大,则C60的硬度也大 |
| C、CO2与SiO2化学式相似,则CO2与SiO2的物理性质也相似 |
| D、Na、K在周期表中属于同一主族,化学性质相似,Na常温下与水剧烈反应,故K常温下也能与水剧烈反应 |
气体甲通入溶液乙中时,随着甲的通入,溶液乙的颜色逐渐褪去,下列说法正确的是( )
| A、气体甲一定具有漂白性 |
| B、溶液乙褪色后,不可能再恢复原来的颜色 |
| C、气体甲一定与溶液乙中的某种有色物质发生化合反应 |
| D、气体甲可能被溶液乙中的某些离子氧化 |
在物质分类中常存在包含关系如图B包含A,下列关系中前者包含后者.其中错误的是( )
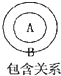

| A、有机物烃 | B、烃脂肪烃 |
| C、脂肪烃烯烃 | D、烯烃氯乙烯 |
归纳与推理是化学学习常用的方法.下列推理正确的是( )
| A、因为稀硫酸能与铁反应放出H2,所以稀硝酸与铁反应也一定能放出H2 |
| B、同族元素具有相似性.因为CaCO3、BaCO3是白色沉淀,所以SrCO3也是白色沉淀 |
| C、蔗糖加入浓硫酸后变黑,说明浓硫酸具有吸水性 |
| D、因为SO2可以使酸性KMnO4溶液褪色,所以SO2具有漂白性 |
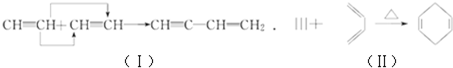
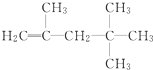 可由(填结构简式)
可由(填结构简式)