题目内容
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.11.2 LCl2通入足量的NaOH 溶液中充分反应 ,转移的电子数为 0.5NA
B.4.4 g 由 CO2 和 N2O 组成的混合气体中含有的电子总数为 2.2NA
C.常温下 ,1.0L p H= l 的 H2SO4溶液中含有H+的数目为 0.2NA
D.11.5 g乙醇分子中含有C- H键的数目为1.5NA
【答案】B
【解析】
A. 氯气所处的状态不明确,无法计算氯气物质的量和电子转移数目,故A错误;
B.CO2 和 N2O的摩尔质量均为44g/mol,故4.4g混合物的物质的量为0.1mol,且两者分子中均含22个电子,故0.1mol混合物中含2.2NA个电子,故B正确;
C. 1.0L p H= l 的 H2SO4溶液中含有H+的数目=1L×0.1mol/L×NA=0.1NA,故C错误;
D.每个乙醇分子(CH3CH2OH)含有5个C- H键,11.5g乙醇分子中含有C- H键的物质的量
![]() ,数目为1.25 NA,故D错误;
,数目为1.25 NA,故D错误;
故选:B。

【题目】现有反应:mA(g)+nB(g)![]() pC(g)
pC(g)
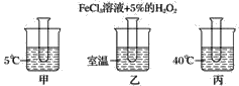
(I)若达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为___热反应,且m+n__p(填“>”、“=”或“<”)。
(2)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色___;而维持容器内压强不变,充入氖气时,混合物颜色___。(填“变深”、“变浅”或“不变”)。
(II)若在容积可变的密闭容器中发生反应,在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如表
压强p/Pa | 2×105 | 5×105 | 1×106 |
c(A)/mol·L-1 | 0.08 | 0.20 | 0.44 |
(1)当压强从2×105Pa增加到5×105Pa时,平衡___移动(填:向左,向右,不)。
(2)维持压强为2×105Pa,当反应达到平衡状态时,体系中共有amol气体,再向体系中加入b molB,当重新达到平衡时,体系中气体总物质的量是___mol。
(3)当压强为1×106Pa时,此反应的平衡常数表达式:___。
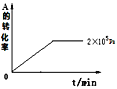
(4)其他条件相同时,在上述三个压强下分别发生该反应。2×105Pa时,A的转化率随时间变化如图,请在图中补充画出压强分别为5×105Pa和1×106Pa时,A的转化率随时间的变化曲线(请在图线上标出压强)。____