题目内容
【题目】 肼(N2H4)具有强还原性,可用作火箭燃料、抗氧剂等。
(1)肼可以由氨气反应制得,已知部分化学键键能如下表所示:
化学键 | H—H | N≡N | N—H |
键能/kJ·molˉ1 | a | b | c |
①工业上合成氨的反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=____ kJ·mol-1
2NH3(g) ΔH=____ kJ·mol-1
②合成氨反应的活化能很大,能加快反应速率但不改变反应活化能的方法是____。
(2)肼作火箭燃料与二氧化氮反应生成氮气和水。已知部分反应热化学方程式如下:
N2(g)+O2(g)=2NO(g) ΔH=+183 kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH=-116.2 kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
写出肼作火箭燃料时反应的热化学方程式____。
(3)肼-空气燃料电池是一种环保型燃料电池,结构如图所示;

①肼-空气燃料电池的负极反应式为____。
②全钒液流可充电电池结构如图所示,将肼-空气燃料电池的A极与全钒液流可充电电池的C极相连,B极与D极相连,写出阴极的电极反应式____。
(4)肼可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。与使用Na2SO3处理水中溶解的O2相比,肼的优点是____。
【答案】3a+b-6c 增大反应物浓度(或升高温度或增大压强) 2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g) ΔH=-1152.8 kJ·mol-1 N2H4+4OH--4e-=N2↑+4H2O VO2++2H++e-=VO2++H2O 处理后无电解质溶液生成,不会腐蚀锅炉
【解析】
(1)①根据ΔH=反应物的键能和-生成物的键能和计算;
②结合影响反应速率的因素温度、压强、浓度和催化剂对反应活化能的影响分析;
(2)已知:①N2(g)+O2(g)=2NO(g) ΔH=+183 kJ·mol-1,②2NO(g)+O2(g)=2NO2(g) ΔH=-116.2 kJ·mol-1,③N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1,由盖斯定律可知③×2-②-①可得2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g),由此计算△H;
(3)①燃料电池的负极发生氧化反应;
②燃烧电池通O2的极为正极,则A极为负极,全钒液流可充电电池的C极相连,则C极为阴极,发生还原反应;
(4)肼的氧化产物为N2,而Na2SO3处理水中溶解的O2的产物为SO42-。
(1)①合成氨的反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=反应物的键能和-生成物的键能和=(bkJ·molˉ1)+(akJ·molˉ1)×3-(ckJ·molˉ1)×6=(3a+b-6c)kJ·mol-1;
2NH3(g) ΔH=反应物的键能和-生成物的键能和=(bkJ·molˉ1)+(akJ·molˉ1)×3-(ckJ·molˉ1)×6=(3a+b-6c)kJ·mol-1;
②影响反应速率的常见因素温度、压强、浓度和催化剂中,只有催化剂能降低反应反应活化能加快反应速率,则能加快反应速率但不改变反应活化能的方法只能是增大反应物浓度或升高温度或增大压强);
(2)已知:①N2(g)+O2(g)=2NO(g) ΔH=+183 kJ·mol-1,②2NO(g)+O2(g)=2NO2(g) ΔH=-116.2 kJ·mol-1,③N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1,由盖斯定律可知:③×2-②-①可得2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g),则△H=(-543 kJ·mol-1)×2-(-116.2 kJ·mol-1)-(+183 kJ·mol-1)=-1152.8 kJ·mol-1,即肼作火箭燃料时反应的热化学方程式为2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g) ΔH=-1152.8 kJ·mol-1;
(3)①燃料电池的负极发生氧化反应,即肼发生氧化反应生成N2,则负极电极反应式为N2H4+4OH--4e-=N2↑+4H2O;
②燃烧电池通O2的极为正极,则A极为负极,全钒液流可充电电池的C极相连,则C极为阴极,发生还原反应,即VO2+得电子发生还原反应生成VO2+,则阴极电极反应式为VO2++2H++e-=VO2++H2O;
(4)使用Na2SO3处理水中溶解的O2产生Na2SO4,易腐蚀锅炉,而肼水中的氧,反应产物为N2和H2O,不会腐蚀锅炉。

【题目】合成氨工业涉及固体燃料的气化,需要研究CO2与CO之间的转化。为了弄清其规律,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g) ![]() 2CO(g) H,测得压强、温度对CO、CO2的平衡组成的影响如图所示,回答下列问题:
2CO(g) H,测得压强、温度对CO、CO2的平衡组成的影响如图所示,回答下列问题:

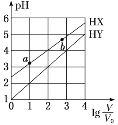
(1)p1、p2、p3的大小关系是________,图中a、b、c三点对应的平衡常数大小关系是______________________。
(2)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:反应1:CO(g)+3H2(g) ![]() CH4(g)+H2O(g) H1= a kJ/mol
CH4(g)+H2O(g) H1= a kJ/mol
反应2:CO(g)+H2O(g) ![]() CO2(g)+H2(g) H2= b kJ/mol
CO2(g)+H2(g) H2= b kJ/mol
① 则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是____________。
② 已知298 K时相关化学键键能数据为:
化学键 | H—H | O—H | C—H |
|
E/(kJ·mol-1) | 436 | 465 | 413 | 1076 |
则根据键能计算,H1=________________。反应1自发进行的条件是___________。(填“较高温度”、“较低温度”、“任意温度”)
(3)一定条件下,CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH3,向固定容积为1 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K =_________(用分数表示);若开始时充入2 mol CH3OH(g) 和2 mol H2O(g)达到相同平衡状态时,CH3OH的转化率为_______;若平衡后再充入4 mol的N2,则c(CO2)和原平衡比较是_________。(填“增大”、“减小”、“不变”)
CH3OH(g)+H2O(g) ΔH3,向固定容积为1 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K =_________(用分数表示);若开始时充入2 mol CH3OH(g) 和2 mol H2O(g)达到相同平衡状态时,CH3OH的转化率为_______;若平衡后再充入4 mol的N2,则c(CO2)和原平衡比较是_________。(填“增大”、“减小”、“不变”)
(4)如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。

①甲中负极的电极反式为_______________,丙中C极的电极反应式为___________。
② 乙中A极析出的气体在标准状况下的体积为__________________。