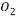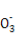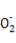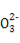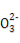ћвƒњƒЏ»Ё
“—÷™25 °ж ±”–єЎ»хЋбµƒµзјл∆љЇв≥£ э»зѕ¬±н:
»хЋб | CH3COOH | HCN | H2CO3 |
µзјл∆љЇв≥£ э(25 °ж) | 1.8°Ѕ10-5 | 4.9°Ѕ10-10 | K1=4.3°Ѕ10-7 K2=5.6°Ѕ10-11 |
‘тѕ¬Ѕ–”–єЎЋµЈ®’э»Јµƒ «(°° °°)
A.a mol/L HCN»№“Ї”лb mol/L NaOH»№“Їµ»ћеїэїмЇѕ,Ћщµ√»№“Ї÷–c(Na+)£Њc(CN-),‘тa“їґ®–°”Џb
B.±щі„Ћб÷–÷рµќЉ”ЋЃ,‘т»№“ЇµƒµЉµз–‘°Ґі„Ћбµƒµзјл≥ћґ»°ҐpHЊщѕ»‘ціуЇуЉх–°
C.Єч»№“ЇpHєЎѕµќ™:pH(Na2CO3)£ЊpH(NaCN)£ЊpH(CH3COONa)
D.‘Џ0.1 mol/L CH3COONa»№“Ї÷–,c(OH-)=c(CH3COOH)+c(H+)
D
°Њљвќц°њAѕо÷–”…c(Na+)£Њc(CN-),ЊЁ»№“Ї÷–µзЇ… ЎЇг÷™c(H+)£Љc(OH-),Ћщ“‘aњ…ƒ№µ»”Џїт–°”Џb,Aѕоін;±щі„Ћб÷–÷рµќЉ”ЋЃ,»№“ЇµƒµЉµз–‘ѕ»‘ціуЇуЉх–°,µзјлґ»‘ціу,pHѕ»Љх–°Їу‘ціу,Bѕоін;Cѕо÷–√ї”–Ћµ√чЄч»№“Їµƒќп÷ µƒЅњ≈®ґ»,є ќёЈ®±»љѕ,Cѕоін;”…÷ „” ЎЇгµ√:c(OH-)=c(CH3COOH)+c(H+),Dѕо’э»Ј°£

ЅЈѕ∞≤бѕµЅ–ір∞Є
ѕаєЎћвƒњ