题目内容
【题目】电化学原理在化学工业中有广泛的应用。请根据如图回答问题:
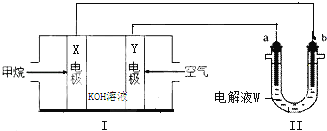
(1)装置Ⅰ中的X电极的名称是____________,Y电极的电极反应式为________,工作一段时间后,电解液的pH将________(填“增大”、“减小”、“不变”)。
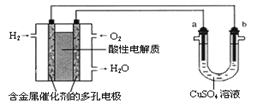
(2)若装置Ⅱ中a、b均为Pt电极,W为饱和食盐水(滴有几滴酚酞),实验开始后,观察到b电极周围溶液变红色,其原因是(用电极反应式表示)___________,a电极上有气泡产生,该气体的电子式为____。
(3)若利用装置Ⅱ进行铜的精炼,则a电极的材料为_______________,工作一段时间后装置Ⅱ电解液中c(Cu2+)将_______________(填“增大”、“减小”、“不变”)。
(4)若装置Ⅱ中a为Ag棒,b为铜棒,W为AgNO3溶液,工作一段时间后发现铜棒增重2.1.6g,则流经电路的电子的物质的量为___________________。
【答案】负极 O2+2H2O+4e﹣=4OH﹣ 减小 2H++2e﹣=H2↑或2H2O+2e﹣=H2↑+2OH﹣ ![]() 粗铜 减小 0.02mol
粗铜 减小 0.02mol
【解析】
(1)装置Ⅰ为甲烷燃料电池,燃料在负极发生氧化反应,生成二氧化碳能够与KOH反应,导致溶液pH减小,在碱性环境中,氧气在正极发生还原反应,生成氢氧根离子,电极反应式为:O2+2H2O+4e-=4OH-;
(2)电解饱和食盐水得到氢气、氯气和氢氧化钠,其离子方程式为:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-,b是阴极,阴极上氢离子放电生成氢气,同时电极附近生成氢氧化钠,所以溶液碱性增强,酚酞试液遇碱变红色,电极反应式为:2H++2e-=H2↑,氯气的电子式为
H2↑+Cl2↑+2OH-,b是阴极,阴极上氢离子放电生成氢气,同时电极附近生成氢氧化钠,所以溶液碱性增强,酚酞试液遇碱变红色,电极反应式为:2H++2e-=H2↑,氯气的电子式为![]() ;
;
(3)电镀法精炼铜时,粗铜为阳极,精铜为阴极,所以阳极材料是粗铜;阳极上失电子变成离子进入溶液,因作阳极的粗铜中的铜和比铜活泼的金属都失去电子进入溶液,阴极溶液中Cu2+得到电子沉积在阴极上,所以,为阳极a电极连接粗铜,电解一段时间后,溶液中铜离子浓度在减小;
(4)铜棒是阴极,银离子放电,生成n(Ag)=![]() =0.02mol,转移电子0.02mol。
=0.02mol,转移电子0.02mol。

【题目】下列根据实验操作和现象所得出的结论正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某溶液中先加入氯水再加入KSCN溶液 | 溶液呈红色 | 原溶液中一定含 |
B | 向盛有 | 试管口出现红棕色气体 |
|
C | 向 | 出现白色胶状沉淀 | 碳的非金属性强于硅的 |
D | 用一束强光照射淀粉溶液 | 产生光亮的“通路” | 淀粉发生水解生成了胶体 |
A.AB.BC.CD.D