题目内容
|
能正确表示下列化学反应的离子方程式是 | |
| [ ] | |
A. |
饱和石灰水跟稀硝酸反应Ca(OH)2+2H+ |
B. |
硫酸铝溶液加过量的氢氧化钠Al3++3OH- |
C. |
将硫酸氢钠滴加到氢氧化钡溶液中至溶液呈中性
|
D. |
用大理石与盐酸制取二氧化碳: |
答案:C
解析:
解析:
|
本题考查的是离子方程式的正确书写.中等难度题.A中对于石灰水的处理不当,如果是参加化学反应,一般写成离子形式,如果是生成物,一般写成化学式;B中由于加入了过量的氢氧化钠,所以一开始生成的氢氧化铝会溶解生成偏铝酸钠;D中大理石不溶于水,只能写成化学式. |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在下列各说法中,正确的是( )
| A、对于2SO2(g)+O2(g)?2SO3(g)△H=-QkJ?mol-1,(Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量一定是Q/2 kJ | B、热化学方程式中的化学计量数不能用分数表示 | C、Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0,该反应的化学能可以转化为电能 | D、△H的大小与热化学方程式的化学计量数无关 |
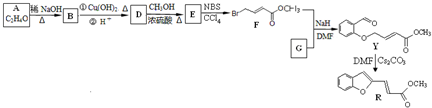
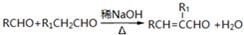 (R、R1表示烃基或氢)
(R、R1表示烃基或氢)
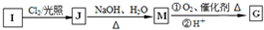


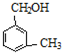 互为同系物
互为同系物