题目内容
将BaO2放入密闭的真空容器中,反应2BaO2(s) 2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
| A.平衡常数减小 | B.BaO量不变 | C.氧气压强不变 | D.BaO2量增加 |
CD
解析试题分析:A.平衡常数只与温度有关,温度不变,平衡常数就不变。错误。B. 该反应的正反应是气体体积增大的反应。保持温度不变,缩小容器容积,也就增大了压强,根据平衡移动原理,化学平衡向气体体积减小的反应,即向逆反应方向移动,所以BaO量减小。错误。C.由于温度不变,化学平衡常数就不变,其数值就等于氧气的浓度,浓度不变,因此压强不变。正确。D. 缩小容器容积,平衡逆向移动,所以体系重新达到平衡BaO2量增加。正确。
考点:考查压强与化学平衡常数及平衡移动的关系的知识。

练习册系列答案
相关题目
在C(s)+CO2(g)===2CO(g)的反应中,现采取下列措施:
①缩小体积,增大压强 ②增加碳的量 ③通入CO2 ④恒容下充入N2
⑤恒压下充入N2能够使反应速率增大的措施是( )
| A.①④ | B.②③⑤ | C.①③ | D.①②④ |
磷酸燃料电池是目前较为成熟的燃料电池之一,其基本组成及反应原理如图所示。
下列说法不正确的是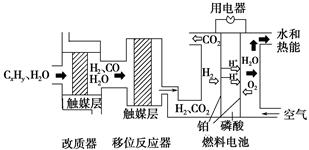
| A.该系统中只存在化学能和电能的相互转化 |
B.在移位反应器中,反应CO(g)+H2O(g) 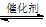 CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大 CO2(g)+H2(g)(ΔH>0),若温度越高,则v(CO)越大 |
| C.改质器和移位反应器的作用是将CxHy转化为H2和CO2 |
| D.该电池正极的电极反应为O2+4H++4e-=2H2O |
已知298 K时,合成氨反应N2(g)+3H2(g)  2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失)
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失)
| A.一定小于92.0 kJ | B.一定大于92.0 kJ |
| C.一定等于92.0 kJ | D.无法确定 |
运用相关化学知识进行判断,下列结论错误的是
| A.某吸热反应能自发进行,因此该反应是熵增反应 |
| B.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
| C.可燃冰主要甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 |
| D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
1000℃时,FeO(s) + H2 Fe(s) + H2O,K=0.52。欲使容器中有1.0 mol FeO被还原,反应前容器中应充入a mol H2。则a最接近
Fe(s) + H2O,K=0.52。欲使容器中有1.0 mol FeO被还原,反应前容器中应充入a mol H2。则a最接近
| A.1.0 | B.2.0 | C.3.0 | D.4.0 |
 2C(气)达到平衡的标志是
2C(气)达到平衡的标志是 2CO(g)反应中可使反应速率增大的措施是
2CO(g)反应中可使反应速率增大的措施是