题目内容
【题目】氮及其化合物的转化是资源利用和环境保护的重要研究课题。
(1)合成氨工业是最基本的无机化工之一,氨是化肥工业和基本有机化工的主要原料。 合成氨反应中有关化学键键能数据如下表:
化学键 | H—H | N≡N | N—H |
E/ kJmol﹣1 | 436 | 946 | 391 |
①已知:合成氨反应:N2(g)+3H2(g)![]() 2NH3(g)的活化能Ea=508 kJmol﹣1,则氨分解反应:2NH3(g)
2NH3(g)的活化能Ea=508 kJmol﹣1,则氨分解反应:2NH3(g)![]() N2(g)+3H2(g)的活化能Ea=_____。
N2(g)+3H2(g)的活化能Ea=_____。
②下图表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:_____(保留3位有效数字)。

③依据温度对合成氨反应的影响,在图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,N2物质的量变化的曲线示意图_______________。

(2)选择性催化还原脱硝技术(SCr)是目前较成熟的烟气脱硝技术,该技术是指在温度300~420℃之间和催化剂条件下,用还原剂(如NH3)选择性地与NOx反应。
①SCr脱硝技术中发生的主要反应为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)△H=-1625.5kJ·mol-1;氨氮比[n(NH3)/n(NO)]会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当n(NH3)/n(NO)>1.0时,烟气中NO浓度反而增大,主要原因是_____。
4N2(g)+6H2O(g)△H=-1625.5kJ·mol-1;氨氮比[n(NH3)/n(NO)]会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,氨气的转化率与氨氮比的关系如图所示。当n(NH3)/n(NO)>1.0时,烟气中NO浓度反而增大,主要原因是_____。

②碱性溶液处理烟气中的氮氧化物也是一种脱硝的方法,写出NO2被Na2CO3溶液吸收生成三种盐的化学反应方程式_____。
③直接电解吸收也被用于脱硝。用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸。电解装置如图所示。阳极的电极反应式为_____。

【答案】 600 kJmol﹣1 14.5% 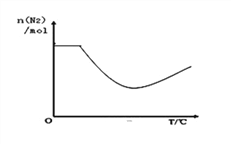 过量氨气与氧气反应生成 NO 2NO2+2Na2CO3+H2O=NaNO3+NaNO2+2NaHCO3 H2O + HNO2 - 2e-= NO3 -+3H+
过量氨气与氧气反应生成 NO 2NO2+2Na2CO3+H2O=NaNO3+NaNO2+2NaHCO3 H2O + HNO2 - 2e-= NO3 -+3H+
【解析】(1)①N2(g)+3H2(g)![]() 2NH3(g)的反应热△H=反应物总键能-生成物总键能=(946+436×3)kJmol﹣1-(6×391)kJmol﹣1=-92 kJmol﹣1,正反应的活化能Ea=508 kJmol﹣1,则逆反应的活化能Ea=(508+92)kJmol﹣1=600kJmol﹣1,即2NH3(g)
2NH3(g)的反应热△H=反应物总键能-生成物总键能=(946+436×3)kJmol﹣1-(6×391)kJmol﹣1=-92 kJmol﹣1,正反应的活化能Ea=508 kJmol﹣1,则逆反应的活化能Ea=(508+92)kJmol﹣1=600kJmol﹣1,即2NH3(g)![]() N2(g)+3H2(g)的活化能Ea=600kJmol﹣11;②设平衡时反应的氮气的物质的量为xmol,则根据方程式可知
N2(g)+3H2(g)的活化能Ea=600kJmol﹣11;②设平衡时反应的氮气的物质的量为xmol,则根据方程式可知
N2(g)+3H2(g)![]() 2NH3(g),
2NH3(g),
起始(mol) 1 3 0
反应(mol) x 3x 2x
平衡(mol) 1-x 3-3x 2x
平衡时氨气的体积分数=![]() =42%,解得x=0.592mol,则N2的平衡体积分数=
=42%,解得x=0.592mol,则N2的平衡体积分数=![]() =14.5%;③N2(g)+3H2(g)
=14.5%;③N2(g)+3H2(g)![]() 2NH3(g)△H= -92 kJmol﹣1,升高温度,平衡逆向移动,N2物质的量增大,因此一定条件下的密闭容器内,从通入原料气开始,随着反应的进行,氮气的物质的量逐渐减小,达到平衡后,随温度不断升高,氮气的物质的量逐渐增大,图像为
2NH3(g)△H= -92 kJmol﹣1,升高温度,平衡逆向移动,N2物质的量增大,因此一定条件下的密闭容器内,从通入原料气开始,随着反应的进行,氮气的物质的量逐渐减小,达到平衡后,随温度不断升高,氮气的物质的量逐渐增大,图像为 ;(2)①4NH3(g)+4NO(g)+O2(g)
;(2)①4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)△H=-1625.5kJ·mol-1,350℃时,只改变氨气的投放量,当n(NH3)/n(NO)>1.0时,过量氨气与氧气反应生成NO,烟气中NO浓度反而增大;②NO2被Na2CO3溶液吸收生成三种盐,二氧化氮与水反应生成一氧化氮和硝酸,一氧化氮和二氧化氮与碱反应能够生成亚硝酸盐,因此反应的化学反应方程式为2NO2+2Na2CO3+H2O=NaNO3+NaNO2+2NaHCO3;③用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸,根据装置图,阳极发生氧化反应,亚硝酸被氧化为硝酸,电极反应式为H2O+HNO2-2e-=NO3-+3H+。
4N2(g)+6H2O(g)△H=-1625.5kJ·mol-1,350℃时,只改变氨气的投放量,当n(NH3)/n(NO)>1.0时,过量氨气与氧气反应生成NO,烟气中NO浓度反而增大;②NO2被Na2CO3溶液吸收生成三种盐,二氧化氮与水反应生成一氧化氮和硝酸,一氧化氮和二氧化氮与碱反应能够生成亚硝酸盐,因此反应的化学反应方程式为2NO2+2Na2CO3+H2O=NaNO3+NaNO2+2NaHCO3;③用6%的稀硝酸吸收NOx生成亚硝酸,再将吸收液导入电解槽电解,使之转化为硝酸,根据装置图,阳极发生氧化反应,亚硝酸被氧化为硝酸,电极反应式为H2O+HNO2-2e-=NO3-+3H+。