题目内容
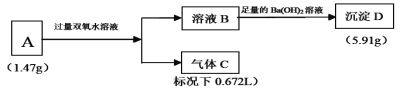
【题目】由三种短周期元素组成的盐A,按如下流程进行实验。溶液B中仅含有2种溶质,其中一种是酸式盐;气体C能使湿润的红色石蕊试纸变蓝。
请回答:
(1)气体C的名称为______,A的化学式为______。
(2)固体A与足量双氧水反应的化学方程式是______。
(3)写出流程图中产生沉淀D的离子方程式______。
【答案】氨气 NaCN NaCN+H2O2+H2O=NaHCO3+NH3↑ Ba2++HCO3-+OH-=BaCO3↓+H2O
【解析】
气体C能使湿润的红色石蕊试纸变蓝,则C为NH3,那么,A中含-3价的N,如果A中N元素以NH4+存在,由于A中只含3种元素,则A中的酸根离子只能为有还原性的S2-或HS-,但是S2-或HS-只能被过氧化氢氧化成S单质,故A中N元素不能以NH4+形式存在,酸根离子也不是S2-或HS-。则A中N元素存在于酸根中,且该酸根具有极强的还原性,符合条件的为CN-,即A中的酸根离子为CN-;
溶液B中仅含有2种溶质,其中一种是酸式盐,由于所加双氧水过量,则溶液B中的一种溶质为H2O2,另一种为碳酸氢盐,沉淀D为BaCO3;
则A中n(C)=n(BaCO3)=![]() =0.03mol,m(C)=12g/mol×0.03mol=0.36g,同理,A中n(N)=n(NH3)=
=0.03mol,m(C)=12g/mol×0.03mol=0.36g,同理,A中n(N)=n(NH3)=![]() =0.03mol,m(N)=14g/mol×0.03mol=0.42g,则A中另一种元素的质量m=1.47g-0.36g-0.42g=0.69g。设组成A的另一种元素为金属元素X,则A为0.03molXCN或0.015molX(CN)2或0.01molX(CN)3,A为XCN时,M(X)=
=0.03mol,m(N)=14g/mol×0.03mol=0.42g,则A中另一种元素的质量m=1.47g-0.36g-0.42g=0.69g。设组成A的另一种元素为金属元素X,则A为0.03molXCN或0.015molX(CN)2或0.01molX(CN)3,A为XCN时,M(X)=![]() ,同理,A为X(CN)2时,M(X)=46g/mol,A为X(CN)3时,M(X)=69g/mol,因为组成A的元素都为短周期元素,则金属元素X的摩尔质量M不可能超过Al的27,则金属元素X的摩尔质量M=23g/mol,即X为Na,故A为NaCN;
,同理,A为X(CN)2时,M(X)=46g/mol,A为X(CN)3时,M(X)=69g/mol,因为组成A的元素都为短周期元素,则金属元素X的摩尔质量M不可能超过Al的27,则金属元素X的摩尔质量M=23g/mol,即X为Na,故A为NaCN;
综上所述,A为NaCN,B为NaHCO3和H2O2的混合溶液,C为NH3,D为BaCO3,据此解答。
(1)由分析可知,C的名称为氨气,A为NaCN,故答案为:氨气;NaCN;
(2)由流程可知,反应物有NaCN和H2O2,生成物有NaHCO3和NH3,结合电子得失守恒、原子守恒可得方程式为:NaCN+H2O2+H2O=NaHCO3+NH3↑,故答案为:NaCN+H2O2+H2O=NaHCO3+NH3↑;
(3)足量Ba(OH)2,HCO3-和OH-以1:1反应生成水和碳酸根离子,碳酸根离子和钡离子结合成碳酸钡,反应的离子方程式为:Ba2++HCO3-+OH-=BaCO3↓+H2O,故答案为:Ba2++HCO3-+OH-=BaCO3↓+H2O。

 考前必练系列答案
考前必练系列答案