��Ŀ����
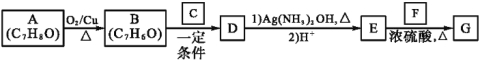
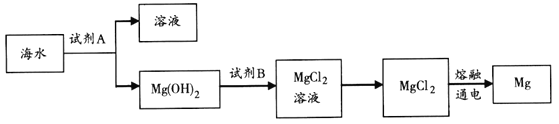
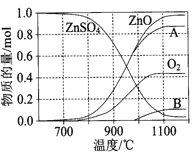
����Ŀ����֪�������ݣ�
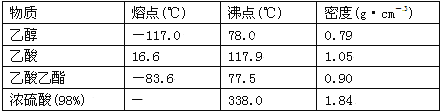
ѧ����ʵ������ȡ������������Ҫ�������£�
����30 mL�Ĵ��Թ�A�а������1��4��4�ı�������Ũ���ᡢ�Ҵ�������Ļ����Һ��
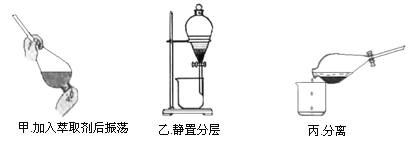
������ͼ���Ӻ�װ��(װ������������)����С����ȵؼ���װ�л����Һ�Ĵ��Թ�5��10 min��

�����Թ�B�ռ���һ�����IJ����ֹͣ���ȣ���ȥ�Թ�B��������Ȼ���ô��ֲ㣻
����������������㡢ϴ�ӡ����
�������ĿҪ��ش��������⣺
��1�����Ƹû����Һ����Ҫ��������Ϊ_______________________��
��2������ʵ���б���̼������Һ��������(����ĸ)__________ __________��
A���к�������Ҵ�
B���к����Ტ���ղ����Ҵ�
C�����������ڱ���̼������Һ�е��ܽ�ȱ���ˮ�и�С�������ڷֲ�����
D�������������ɣ���������
��3������������ҪС����ȼ��Ȳ���������Ҫ������________________________��
��4�����������������Ϊ�˸�������������ѡ�õĸ����Ϊ(����ĸ)______��
A��P2O5 B����ˮNa2SO4
C����ʯ�� D��NaOH����
��5��Ũ����������ǣ��� ���� ��
��6��װ����ͨ�����ĵ���Ҫ���ڱ���̼������Һ��Һ���ϣ����ܲ�����Һ�У�Ŀ���Ƿ�ֹ ��
��7����Ҫ���Ƶõ������������������Ӧ���õ�ʵ������� ��
��8��ijͬѧ���ռ����������������뱥��NaHCO3��Һ�У��۲쵽���������ݲ������ɵó��Ľ����� ���ù����з�����Ӧ�Ļ�ѧ����ʽ�� ��
���𰸡�
��1���ڴ��Թ����ȼ�4 mL�Ҵ����ٻ�������1 mLŨH2SO4���ӱ������������º��ټ�4 mL���Ტҡ�ȣ�
��2��BC
��3����ֹ��Ӧ����������һ�������������������ԭ����ʧ������������Ӧ
��4��B
��5�������ã���ˮ����
��6������
��7���ñ���̼������Һ�н�������������������ٷ�Һ
��8�������������������CH3COOH+NaHCO3=CH3COONa+CO2��+H2O
��������
�����������1��Ũ�����ܶȴ���ˮ��������ˮ�ų������ȣ�Ӧ�ý�Ũ��������Ҵ��У���ȷ��������Ϊ����ŨH2SO4�����Ҵ��У��ӱ���Ȼ���ټ��������2���Ʊ���������ʱ���ñ���̼������Һ��������������Ŀ���dz�ȥ�Ҵ������ᡢ���������������ܽ�ȣ����ڷֲ㡣��ѡBC����3���Ҵ�������ķе�ϵͣ�Ϊ��ֹ�Ҵ�������ӷ���ӦС����ȣ����������ԭ�ϵ���ʧ���ʴ�Ϊ����Ӧ�����Ҵ�������ķе�ϵͣ����ô����ȣ�������Ӧ���������������ʧԭ�ϣ��¶ȹ������ܷ�����������Ӧ����4����ˮ��������ˮ�γ������ƽᾧˮ�������ѡ��P2O5����ʯ�Һ�NaOH�ȹ����������Է��������������ԣ�P2O5��ˮ�����ᣩ�����������ˮ�⣬��ѡB����5��Ũ������������Ӧ�е�����Ϊ�����ú���ˮ���á���6�����ܲ��ܲ���Һ��������Ϊ�˷�ֹ��������7���ñ���̼������Һ�н��������������������Ӧ�����ᣬ�ܽ��Ҵ����ٷ�Һ����8�������̼���Ʒ�Ӧ���ɶ�����̼������ʽΪ�� CH3COOH+NaHCO3=CH3COONa+CO2��+H2O��

 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д�