题目内容
8.将浓硫酸下列性质的代号,填入各小题后面对应的括号中:A.脱水性; B.强酸性; C.难挥发性; D.氧化性; E.吸水性
(1)将胆矾放入装有浓H2SO4的干燥器中,过一段时间胆矾变白色.E
(2)在烧杯中放入蔗糖,滴入浓H2SO4变黑,并产生大量气体.AD
(3)用稀硫酸清洗金属表面的氧化物B.
分析 (1)浓硫酸具有吸水性能够吸收晶体中的结晶水;
(2)浓硫酸具有脱水性,能够使蔗糖炭化,浓硫酸具有强的氧化性,能够氧化碳生成二氧化碳;
(3)浓硫酸具有酸性能够与金属氧化物反应生成盐和水.
解答 解:(1)将胆矾放入装有浓H2SO4的干燥器中,过一段时间胆矾变白色.是因为浓硫酸吸收了胆矾中的结晶水,体现了吸水性;
故答案为:E;
(2)在烧杯中放入蔗糖,滴入浓H2SO4变黑,是因为浓硫酸将蔗糖中的H、O元素脱去生成水,体现了脱水性.同时浓硫酸与生成的碳反应,体现了强氧化性;
故答案为:AD;
(3)用稀硫酸清洗金属表面的氧化物,利用的稀硫酸的酸性,故答案为:B.
点评 本题考查了物质的性质,熟悉浓硫酸的吸水性、脱水性和强氧化性、酸性是解题关键,注意浓硫酸吸水性与脱水性的区别.

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
3.下表是元素周期表的一部分,针对表中所列标号为①~⑩的元素回答下列问题.
(1)非金属性最强的元素是F(填元素符号),形成化合物种类最多的元素是C(填元素符号).
(2)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式),具有两性的是Al(OH)3(填化学式).
(3)⑤⑥⑦三元素的金属性强弱顺序为Na>Mg>Al(填元素符号),判断的实验依据是单质与水或酸反应的剧烈程度(写出一种).
(4)元素⑨的原子结构示意图为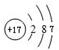 ;元素③的最低价氢化物的电子式为
;元素③的最低价氢化物的电子式为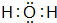 .
.
| 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)第三周期元素除⑩外原子半径最小的是Cl(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是NaOH(填化学式),具有两性的是Al(OH)3(填化学式).
(3)⑤⑥⑦三元素的金属性强弱顺序为Na>Mg>Al(填元素符号),判断的实验依据是单质与水或酸反应的剧烈程度(写出一种).
(4)元素⑨的原子结构示意图为
 ;元素③的最低价氢化物的电子式为
;元素③的最低价氢化物的电子式为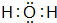 .
.
13.某兴趣小组为研究电池原理,设计如图装置.以下叙述不正确的是( )
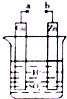

| A. | a和b不连接时,无电流产生,Zn片表面有气泡逸出 | |
| B. | a和b用导线连接,有电流产生,Cu片表面有气泡逸出 | |
| C. | 无论a和b是否连接,Zn片均被腐蚀,溶液的pH均减小 | |
| D. | 若将装置中H2SO4溶液换成CuSO4溶液仍然可以设计成原电池 |
20.下列物质的水溶液呈碱性的是( )
| A. | FeCl3 | B. | KSCN | C. | CH3COOH | D. | NH4Al(SO4)2 |
17.硫氰[(SCN)2]的化学性质和卤素(X2)类似,称为拟卤素,如(SCN)2+H2O═HSCN+HSCNO,它们的阴离子的还原性强弱为Cl-<Br-<SCN-<I-.下列说法不正确的是( )
| A. | Cl2可以与KSCN溶液反应 | B. | (SCN)2可以与KI溶液反应 | ||
| C. | KSCN溶液可以与FeCl3溶液反应 | D. | (SCN)2可以与KBr溶液反应 |
18.下列变化需要加入适当的氧化剂才能完成的是( )
| A. | Fe→Fe3O4 | B. | HNO3→NO | C. | H2SO4 →CuSO4 | D. | Na2O→NaOH |
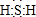 .
.