题目内容
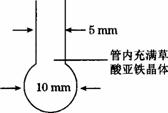
某化学学习小组同学根据实验室现有的制取氨气的药品,设计了右图所示的实验装置(部分夹持仪器未画出),制取并探究氨气的还原性、检验反应产物。请回答下列问题:
(1)A中发生反应的化学方程式是 。
(2)B中碱石灰的作用是 。
(3)C中黑色固体变红,且产生的气体对空气无污染,写出该反应的化学方程式 ;D中发生的现象是__________________________。
(4)该装置存在明显缺陷,该缺陷是 。
(5)工业中常用氮气与氢气在高温、高压、铁触媒做催化剂的条件下合成氨气,该小组同学模拟该条件也合成出了氨气。已知起始时,将2 mol N2、6 mol H2充入一个容积为2 L的密闭容器中发生反应,过了5 min后,混合气体的总物质的量减少了1 mol,求在这段时间内以H2表示的化学反应速率为 。

(1)Ca(OH)2+2NH4Cl = CaCl2+2NH3↑+2H2O(2分);
(2)干燥氨气(1分); (3)3CuO + 2NH3 3Cu + N2 + 3H2O(2分);
(4)无水硫酸铜变蓝(1分);缺少尾气处理装置(1分); (5)0.15 mol/(L·min)(2分);

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目

 这样便得到了高纯度的纳米铁粉.
这样便得到了高纯度的纳米铁粉. Fe+2CO2↑+2H2O↑
Fe+2CO2↑+2H2O↑