��Ŀ����
��10�֣����ᷢ��������ԭ��Ӧ��ʱ��һ������Ũ��Խϡ����Ӧ��ԭ�����е��Ļ��ϼ�Խ�͡�����������һ���������ۺ����۵Ļ������һ������ϡ��HNO3��ַ�Ӧ����Ӧ���������κ�����ų����ڷ�Ӧ���������Һ�У���μ���4mol /LNaOH��Һ������NaOH��Һ�������mL����������������ʵ�����mol����ϵ��ͼ��ʾ����

��1��B��A�IJ�ֵ�� mol��
��2��B����ֵ�� mol��
��3��C����ֵ�� mL����Ҫ���м�����̣�

��1��B��A�IJ�ֵ�� mol��
��2��B����ֵ�� mol��
��3��C����ֵ�� mL����Ҫ���м�����̣�
0.008 0.032 7
������֪�����������ᷴӦʱ������Ļ�ԭ����ΪNH4NO3����ͼ�ֿɿ������������ᷴӦ�������ǹ����ģ��ʽ�������������ΪFe(NO3)3��Al(NO3)3��ͼ�У���0��C��H++OH��=H2O����C��31��R3++3OH��=R(OH)3����R����Fe��Al������31��34��NH4++ OH��=NH3?H2O����34��36��Al(OH)3+ OH��=AlO2��+ 2H2O���ɢ�֪n[Al(OH)3]=0.002L��4mol��L��1=0.008mol=n(Al)����ֵҲ��B��A�IJ�ֵ���ɢ�֪��n(NH4NO3)=0.003L��4mol��L��1=0.012mol�����ݷ�Ӧ�е�ʧ������ȵ�ԭ��ã�3n(R3+)="0.012��8=0.096" mol����n(R3+)=0.032mol=n(�Ͻ�)���ʻ������n(Al):n(Fe)=1:3��0��31mL�У����ڳ����������ӵ�OH����0.032 mol��3="0.096" mol����C�㣺(0.031L��4 mol��L��1��0.096 mol)��4 mol��L��1=0.007L����7mL��

��ϰ��ϵ�д�
�����Ŀ

 ��HCO��3����Ϊ0��1 NA
��HCO��3����Ϊ0��1 NA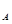 ��ʾ�����ӵ�������ֵ������������ȷ����( )
��ʾ�����ӵ�������ֵ������������ȷ����( )  �����������Ӻ������ӵ�����Ϊ0.03 N
�����������Ӻ������ӵ�����Ϊ0.03 N ����������ͭ��Ӧ,����
����������ͭ��Ӧ,���� �ķ�����Ϊ0.92 N
�ķ�����Ϊ0.92 N ��Һ����������С��3N
��Һ����������С��3N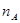 ��ʾ�����ӵ�������ֵ������������ȷ����
��ʾ�����ӵ�������ֵ������������ȷ���� �к��еĵ�����Ϊ
�к��еĵ�����Ϊ �к��е�ԭ����Ϊ
�к��е�ԭ����Ϊ ����Һ�е������
����Һ�е������ ��Ϊ
��Ϊ ���к��еķ�����Ϊ
���к��еķ�����Ϊ