题目内容
相同条件下,分别向10mL0.1mol?L-1的盐酸、硫酸、醋酸溶液中加入足量的Zn充分反应后产生H2的量是( )
分析:盐酸、醋酸为一元酸,硫酸为二元酸,与足量的Zn反应时,硫酸生成氢气较多,以此解答.
解答:解:三种酸中,盐酸和醋酸为一元酸,与锌完全反应时,生成的氢气相同,而硫酸为二元酸,与足量的Zn反应生成的氢气为盐酸、醋酸的物质的量的二倍,
故选B.
故选B.
点评:本题考查酸与金属的反应,侧重于学生的分析能力的考查,为高频考点,注意把握酸的分类和性质,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 图中,P为可自由滑动的活塞,关闭K,V(A)=aL,V(B)=0.8aL(连通管的体积忽略不计).在相同温度和有催化剂存在的条件下,分别向容器A、B中各充入1molN2和3molH2,发生反应N2(g)+3H2(g)
图中,P为可自由滑动的活塞,关闭K,V(A)=aL,V(B)=0.8aL(连通管的体积忽略不计).在相同温度和有催化剂存在的条件下,分别向容器A、B中各充入1molN2和3molH2,发生反应N2(g)+3H2(g)  2NH3(g);△H=-92.4kJ/mol.达到平衡后,V(B)=0.6aL.
2NH3(g);△H=-92.4kJ/mol.达到平衡后,V(B)=0.6aL.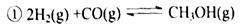

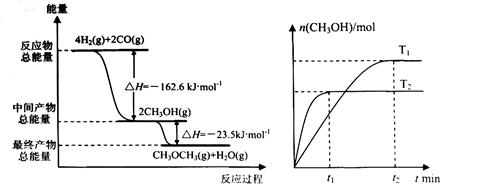
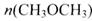 =_________mol。
=_________mol。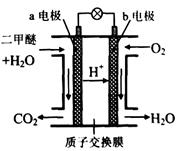



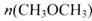 =_________mol。
=_________mol。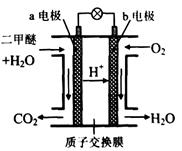
 2NH3(g);△H=-92.4kJ/mol.达到平衡后,V(B)=0.6aL.
2NH3(g);△H=-92.4kJ/mol.达到平衡后,V(B)=0.6aL.