题目内容
下列叙述不正确的是( )
| A.化学平衡发生移动,平衡常数不一定发生变化 |
| B.升高温度会增大化学反应速率,其原困是增加了活化分子的百分数 |
C.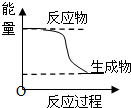 某化学反应的能量变化如图所示,则该反应的△H>0.△S>0 |
| D.H3PO4的电离常数:Kal>>Ka2>>Ka3 |
A、浓度、压强改变,平衡移动,平衡常数不发生变化;温度改变,平衡移动,平衡常数一定发生变化,所以化学平衡发生移动,平衡常数不一定发生变化,故A正确;
B、升高温度会增大化学反应速率,其原困增加了活化分子的百分数,故B正确;
C、反应物的总能量大于生成物的总能量,反应放热,△H<0,无法物质的状态和化学计量数,不能判断熵变,故C错误;
D、由于电离生成氢离子,抑制第二步电离、第三步电离,则H3PO4的电离常数:Kal>>Ka2>>Ka3,故D正确;
故选:C.
B、升高温度会增大化学反应速率,其原困增加了活化分子的百分数,故B正确;
C、反应物的总能量大于生成物的总能量,反应放热,△H<0,无法物质的状态和化学计量数,不能判断熵变,故C错误;
D、由于电离生成氢离子,抑制第二步电离、第三步电离,则H3PO4的电离常数:Kal>>Ka2>>Ka3,故D正确;
故选:C.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目