题目内容
一定温度下,在 2L的密闭容器中发生如下反应:A(s)+2B(g) xC(g)△H<0,B、C的物质的量随时间变化的关系如下图(左),达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如下图(右)。下列有关说法正确的是( )
xC(g)△H<0,B、C的物质的量随时间变化的关系如下图(左),达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如下图(右)。下列有关说法正确的是( )
A.x=2.反应开始2min内,v(A)="0.05" mol·L-1·min-1
B.tl时改变的条件是降温,平衡逆向移动
C.t2时改变的条件可能是增大c的浓度,t2时正反应速率减小
D.t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变
D
解析试题分析:通过左图可知,2min达平衡,△n(B)=0.3mol-0.1mol=0.2mol,△n(C)=0.2mol,物质的量变化量之比等于化学计量数之比,故2:x=0.2mol:0.2mol,解得x=2,v(B)=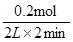 =0.5 mol/(L?min)。但A是固体,不能表示反应速率,故A错误;正反应为放热反应,当降低温度,反应正向移动,正逆速率都减小,并且正反应速度降低的幅度更大,故B错误;当增加c(C),反应逆向移动,反应速率增大,且逆反应的速率增加幅度更大,故C不正确;反应前后气体的物质的量不变,减小压强,同等程度降低速率,平衡不移动,使用催化剂,同等程度加快反应速率,平衡不移动,故D正确,答案选D。
=0.5 mol/(L?min)。但A是固体,不能表示反应速率,故A错误;正反应为放热反应,当降低温度,反应正向移动,正逆速率都减小,并且正反应速度降低的幅度更大,故B错误;当增加c(C),反应逆向移动,反应速率增大,且逆反应的速率增加幅度更大,故C不正确;反应前后气体的物质的量不变,减小压强,同等程度降低速率,平衡不移动,使用催化剂,同等程度加快反应速率,平衡不移动,故D正确,答案选D。
考点:考查化学反应速率和化学平衡的图象问题
点评:该题是高考中的常见题型,属于中等难度的试题,试题针对性强,贴近高考,注重对学生能力的培养,有利于培养学生的逻辑推理能力和抽象思维能力。注意右图中纵坐标是表示逆反应速率,注意条件变化逆反应速率随实际变化。

一定温度下的定容容器中,反应A2(g)+B2(g) 2AB(g)达到平衡标志的是 ( )
2AB(g)达到平衡标志的是 ( )
| A.单位时间内生成2n mol AB同时消耗n mol B2 |
| B.单位时间总物质的量不随时间的变化而变化 |
| C.单位时间内生成n mol A2同时消耗n mol B2 |
| D.容器内各组分的物质的量不随时间的变化而变化 |
向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时, 按正反应速率由大到小的顺序排列,正确的是
①500 ℃, 10 mol SO2和5 mol O2反应
②500 ℃, 用V2O5作催化剂, 10 mol SO2和5 mol O2反应
③450 ℃, 8 mol SO2和5 mol O2反应
④500 ℃, 8 mol SO2和5 mol O2反应。
| A.②①④③ | B.②①③④ | C.①②③④ | D.④③②① |
某反应中,X、Y、Z三种物质的物质的量随时间的变化如图所示。下列说法正确的是
| A.反应为 X + 2Z= Y |
B.反应为 X + Y 2Z 2Z |
| C.4 s 时,反应达到平衡 |
| D.12 s 时,反应不再进行 |
在一密闭容器中充入1molNO2气体,建立如下平衡2NO2  N2O4,测得NO2转化率为a%。在温度、体积不变时,再通入1molNO2,待新平衡建立时,测得NO2的转化率为b%, a与b比较
N2O4,测得NO2转化率为a%。在温度、体积不变时,再通入1molNO2,待新平衡建立时,测得NO2的转化率为b%, a与b比较
| A.a>b | B.b>a | C.a=b | D.无法比较 |
在一定条件下,将 两种气体通入密闭容器中,反应按
两种气体通入密闭容器中,反应按

 进行,2秒钟后反应速率如下:
进行,2秒钟后反应速率如下: ,
, ,
, ,则x、y的值分别为( )
,则x、y的值分别为( )
| A.3和2 | B.1和3 | C.3和1 | D.4和5 |
某可逆反应L(s) + G(g)  3R(g) △H>0,下图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示( )
3R(g) △H>0,下图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示( )
| A.平衡混合气中R的质量分数 | B.达到平衡时G的转化率 |
| C.平衡混合气中G的质量分数 | D.达到平衡时L的转化率 |
 2C(g),平衡后增大压强,A的百分含量减小,则n≥2。
2C(g),平衡后增大压强,A的百分含量减小,则n≥2。 2SO3(g)2 min末测得容器中有7.2 mol SO2。试回答:
2SO3(g)2 min末测得容器中有7.2 mol SO2。试回答: 葡萄糖
葡萄糖 CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动) 人体所需的蛋白质(人体生长发育、新陈代谢)
人体所需的蛋白质(人体生长发育、新陈代谢)