题目内容
在一密闭容器中充入1molNO2气体,建立如下平衡2NO2  N2O4,测得NO2转化率为a%。在温度、体积不变时,再通入1molNO2,待新平衡建立时,测得NO2的转化率为b%, a与b比较
N2O4,测得NO2转化率为a%。在温度、体积不变时,再通入1molNO2,待新平衡建立时,测得NO2的转化率为b%, a与b比较
| A.a>b | B.b>a | C.a=b | D.无法比较 |
B
解析试题分析:第一次达平衡后,再加入NO2,由于该容器是一个固定容积的密闭容器,所以加入NO2后,反应体系的压强增大;增大压强,化学平衡向气体体积减小的方向移动,所以平衡向正反应方向移动,NO2的转化率增大,即b>a,答案选B。
考点:考查外界条件对平衡状态对影响
点评:本题以二氧化氮和四氧化二氮的可逆反应为载体考查了化学平衡移动原理,要注意:压强只对反应前后气体体积改变的可逆反应平衡移动有影响,对反应前后气体体积不变化的可逆反应无影响,但压强对所有有气体参加的可逆反应反应速率都有影响,无论反应前后气体体积是否变化。

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
下列反应中产生气泡速率最快的是
| | 温度 | 浓度 | 催化剂 |
| A | 25℃ | 2mL5%H2O2 | 0.1mol/LFeCl32滴 |
| B | 35℃ | 2mL8%H2O2 | MnO2粉末 |
| C | 25℃ | 2mL5%H2O2 | MnO2粉末 |
| D | 25℃ | 2mL8%H2O2 | 0.1mol/LCuCl22滴 |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2 2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
2SO3,这是一个放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中,错误的是
| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.达到平衡时,改变反应条件可能在一定程度上改变该反应的化学平衡状态 |
| D.达到平衡时,SO2的浓度与SO3的浓度一定相等 |
为探究足量锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是( )
| A.加入NH4HSO4固体,v(H2)不变,生成H2量不变 |
| B.加入少量水,v(H2)减小,生成H2量减少 |
| C.加入CH3COONa固体,v(H2)减小,生成H2量不变 |
| D.滴加少量CuSO4溶液,v(H2)增大,生成H2量减少 |

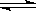 3C (g) 。下列叙述中表明该可逆反应一定达到平衡状态的是
3C (g) 。下列叙述中表明该可逆反应一定达到平衡状态的是 xC(g)△H<0,B、C的物质的量随时间变化的关系如下图(左),达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如下图(右)。下列有关说法正确的是( )
xC(g)△H<0,B、C的物质的量随时间变化的关系如下图(左),达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如下图(右)。下列有关说法正确的是( )
 N2O4,此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是( )
N2O4,此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是( )