��Ŀ����
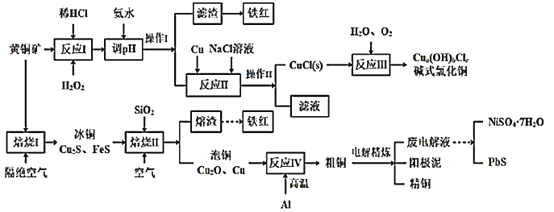
����Ŀ����������һ����Ҫ�Ļ����м��壬������ҵ�о����ȵ㡣һ���Ը����̿�(��Ҫ�ɷ�Ϊ���̻����PFeS)Ϊԭ���Ʊ������̵Ĺ����������£�
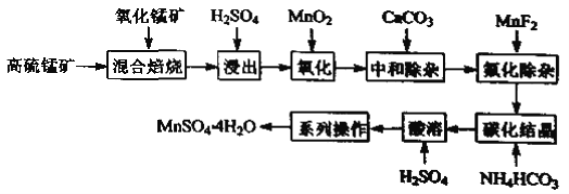
��֪��������ϱ�������������MnSO4��Fe2O3������FeO��Al2O3��MgO��
�ڽ���������ˮ��Һ�е�ƽ��Ũ����pH�Ĺ�ϵ��ͼ��ʾ(25��)��
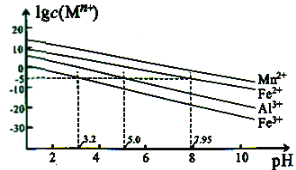
�۴�ʵ��������Mn2+��ʼ������pHΪ7.54��������Ũ����105mol��L1ʱ������Ϊ���ӳ�����ȫ��
��ش�
��1����ͳ���մ��������̿�ʱ����������ϱ�����������ֱ����H2SO4��������ȱ��Ϊ____��
��2����������ʱ��������Ӧ�����ӷ���ʽΪ____����ʡ�������������裬��ɵĺ����____��
��3�����кͳ�����ʱ�����ɳ�������Ҫ�ɷ�Ϊ____(�ѧʽ)��
��4��������������ʱ����ʹ��Һ�е�Mg2+��Ca2+������ȫ����ά��c(F-)������____��(��֪��Ksp(MgF2)=6.4��1010��Ksp(CaF2)=3.6��1012)
��5����̼���ᾧ��ʱ��������Ӧ�����ӷ���ʽΪ_____��
��6���ö��Ե缫���MnSO4��Һ���Ʊ�MnO2���������������ĵ缫��ӦʽΪ____��
���𰸡�������������壬��Ⱦ���� MnO2+2Fe2++4H+=2Fe3++Mn2++2H2O Fe2+��Mn2+���������ص������Mn2+��ʧ(��Fe2+ȥ������ȫ,Ӱ���Ʒ����) Fe(OH)3��Al(OH)3 8��103mol��L1 Mn2++2HCO3-=MnCO3��+CO2��+H2O Mn2++2H2O2e=MnO2+4H+
��������
�����̿���Ҫ�ɷ�Ϊ���̻����PFeS���������̿��ϱ��գ��õ�MnSO4��Fe2O3������FeO��Al2O3��MgO���������ᣬ�õ�Mn2+��Fe2+��Fe3+��Mg2+��Al3+��������Һ������������̽�������������Ϊ�����ӱ��ڳ�ȥ���ټ���̼����кͣ������������������������������ʽ��ȥ������MnF2���ӣ�ʹ��Һ�е�Mg2+������ȫ����ʱ��Һ�еĽ�������Ϊ�����ӣ�����̼��立���Mn2++2HCO3-=MnCO3��+CO2��+H2O�����������ܽ������̣���������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����õ������̵�ˮ����ݴ˷�����
��1�����̿���FeS����ͳ���մ��������̿�ʱ����������ϱ�����������ֱ����H2SO4������������������壬��Ⱦ�������ʴ�Ϊ��������������壬��Ⱦ������
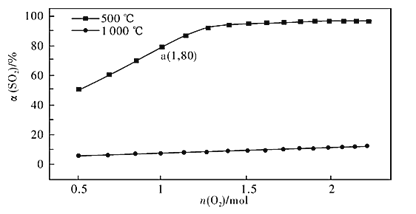
��2������ʱ�ö������������������ӣ����ӷ���ʽΪ��MnO2+2Fe2++4H+=2Fe3++Mn2++2H2O����ʡ�������������裬����ͼ��Fe2+��Mn2+���������ص������Mn2+��ʧ(��Fe2+ȥ������ȫ��Ӱ���Ʒ����)���ʴ�Ϊ��MnO2+2Fe2++4H+=2Fe3++Mn2++2H2O��Fe2+��Mn2+���������ص������Mn2+��ʧ(��Fe2+ȥ������ȫ,Ӱ���Ʒ����)��
��3�����кͳ�����ʱ����������������������̼�������֮�䷢��˫ˮ�ⷴӦ�õ�Fe(OH)3��Al(OH)3�������ʴ�Ϊ��Fe(OH)3��Al(OH)3��
��4����֪��Ksp(MgF2)=6.4��1010����ʹ��Һ�е�Mg2+������ȫ����ά��c(F)������![]() ���ʴ�Ϊ��8��103mol��L1��
���ʴ�Ϊ��8��103mol��L1��
��5����̼���ᾧ��ʱ��������Ӧ�����ӷ���ʽΪ��Mn2++2HCO3-=MnCO3��+CO2��+H2O��
�ʴ�Ϊ��Mn2++2HCO3-=MnCO3��+CO2��+H2O��
��6���ö��Ե缫���MnSO4��Һ���Ʊ�MnO2������������������������Ӧ��Ԫ�ػ��ϼ����ߣ���Ϊ������ʧȥ�������ɶ������̣��缫��ӦʽΪ��Mn2++2H2O2e=MnO2+4H+���ʴ�Ϊ��Mn2++2H2O2e=MnO2+4H+��

 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�����Ŀ����������Ⱦ����Դ��ȱ��������ͻ������Դ��ѭ��������Ϊ��Ҫ����ҵ �����ú� Cu2O�������� Al2O3��Fe2O3 �� SiO2���Ŀ�����ȡͭ�Ĺ����������£�
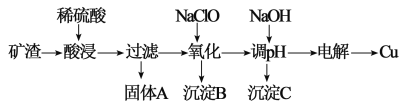
��֪����Cu2O ��������������ת���ɵ��� Cu �ͺ� Cu2+����Һ��
�ڼ��������������ʱ�� pH ���±���
�������� | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 |
����ʱ�� pH | 4.0~5.2 | 5.8~8.8 | 1.1~3.2 | 5.4~6.7 |
�ش��������⣺
��1���������� A ���еijɷ�Ϊ Cu ����һ�����ʣ��ӹ��� A �з���� Cu �Ŀ� ���Լ�Ϊ_____��Һ���ѧʽ����
��2����������������ˡ�ϴ�Ӻ���Ԫ�ص���Ҫ������ʽΪ__________�����ӷ��ţ�����������ӵij��û�ѧ�Լ���_________________��
��3���� NaClO ������������Һ�� pH Ϊ_____���õ����� B ��һ�־���Ư�� �Ե����� D���÷�Ӧ���ӷ���ʽΪ_________��
��4��25��ʱ���� NaOH ���������Һ pH �õ� Al(OH)3 �������� pH=5.3 ʱ������ ��Һ�� c(Al3+)=_____����֪ 25��ʱ Ksp[Al(OH)3]=1.3��10-33��
��5���ö��Ե缫����ý���ͭʱ����ʼ������������������������ʵ���֮��Ϊ___________��