题目内容
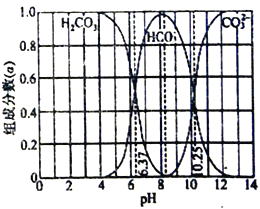
【题目】25℃时,改变0.1mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数![]() (X)随pH的变化如图所示[已知
(X)随pH的变化如图所示[已知![]() (X)=
(X)= ]。
]。

下列叙述错误的是
A. Ka1(H2A)的数量级为10-2
B. pH=4.2时,c(HA-)=c(A2-)>c(H+)
C. NaHA溶液中,HA-的电离平衡常数大于HA-的水解平衡常数
D. 在含H2A、HA-和A2-的溶液中,若c(H2A)+2c(A2-)+c(OH-)=c(H+)则![]() (H2A)和
(H2A)和![]() (HA-)一定相等
(HA-)一定相等
【答案】D
【解析】由图像可知,pH=1.2时,c(H2A)=c(HA-),pH=2.7时,c(H2A)=c(A2-),pH=4.2时,c(HA-)=c(A2-),随着pH的增大,c(H2A)逐渐减小,c(HA-)先增大后减小,c(A2-)逐渐增大。A.pH=1.2时,c(H+)=10-1.2mol/L,c(HA-)= c(H2A),K1(H2A)=  =10-1.2,Ka1(H2A)的数量级为10-2,故A正确;B.pH=4.2时,c(HA-)= c(A2-)≈0.05 mol/L,c(H+)=10-4.2mol/L,因此c(HA-)=c(A2-)>c(H+),故B正确;C.pH=4.2时,即HA-电离出氢离子使溶液呈酸性,则c(H+)>c(OH-),故HA-的水解能力小于HA-的电离能力,故C正确;D.如果
=10-1.2,Ka1(H2A)的数量级为10-2,故A正确;B.pH=4.2时,c(HA-)= c(A2-)≈0.05 mol/L,c(H+)=10-4.2mol/L,因此c(HA-)=c(A2-)>c(H+),故B正确;C.pH=4.2时,即HA-电离出氢离子使溶液呈酸性,则c(H+)>c(OH-),故HA-的水解能力小于HA-的电离能力,故C正确;D.如果![]() (H2A)=
(H2A)= ![]() (HA-),则c(H2A)=c(HA-),根据图像,pH=1.2,此时溶液中几乎没有A2-,与题意不符,故D错误;故选D。
(HA-),则c(H2A)=c(HA-),根据图像,pH=1.2,此时溶液中几乎没有A2-,与题意不符,故D错误;故选D。

练习册系列答案
相关题目