题目内容
17.下列物质:①锌 ②CuSO4•5H2O ③BaCO3 ④乙醇 ⑤SO2 ⑥H2SO4⑦KNO3溶液 ⑧KOH. 其中属于电解质的是(填物质序号)②③⑥⑧.写出下列反应的离子方程式:
(1)①与②的水溶液反应:Zn+Cu2+=Zn2++Cu;
(2)①与⑥的稀溶液反应:Zn+2H+=Zn2++H2↑;
(3)③与⑥的稀溶液反应:BaCO3+2H++SO42-=BaSO4↓+H2O+CO2↑;
(4)②的水溶液与⑧的水溶液反应:Cu2++2OH-═Cu(OH)2↓;
(5)将⑧的固体露置空气中一段时间使其部分变质后,配成溶液与⑥的稀溶液(足量)反应:CO32-+2H+=H2O+CO2↑;H++OH-=H2O.
分析 电解质指:水溶液中或熔融状态下能够导电的化合物,注意能导电,必须是电解质自身电离出自由移动的离子;在上述两种情况下都不能导电的化合物称为非电解质;
(1)锌与硫酸铜溶液反应置换出铜;
(2)锌与稀硫酸反应生成硫酸锌和氢气;
(3)碳酸钡与硫酸反应生成硫酸钡和二氧化碳和水;
(4)硫酸铜溶液与氢氧化钾溶液发生复分解反应生成硫酸钾和氢氧化铜沉淀;
(5)氢氧化钾能够吸空气中的二氧化碳生成碳酸钾和水,部分变质的氢氧化钾含有碳酸钾、氢氧化钾,碳酸钾与硫酸反应生成二氧化碳和水、硫酸钾;氢氧化钾与稀硫酸反应生成硫酸钾和水.
解答 解:①锌是单质,不属于电解质;
②CuSO4•5H2O 是水溶液中或熔融状态下能够导电的化合物,属于电解质;
③BaCO3 熔融状态下能够导电,属于电解质;
④乙醇 水溶液中和熔融状态下都不导电的化合物,属于非电解质;
⑤SO2 本身不能电离产生自由离子,属于非电解质;
⑥H2SO4水溶液中能够导电的化合物,属于电解质;
⑦KNO3溶液属于混合物,不是电解质;
⑧KOH是水溶液中或熔融状态下能够导电的化合物,属于电解质;
故答案为:②③⑥⑧;
(1)锌与硫酸铜溶液反应置换出铜,离子反应为Zn+Cu2+=Zn2++Cu,
故答案为:Zn+Cu2+=Zn2++Cu;
(2)锌与硫酸反应生成硫酸锌和氢气,离子方程式:Zn+2H+=Zn2++H2↑;
故答案为:Zn+2H+=Zn2++H2↑;
(3)碳酸钡与稀硫酸反应反应生成硫酸钡和二氧化碳和水,BaCO3+2H++SO42-=BaSO4↓+H2O+CO2↑;
故答案为:BaCO3+2H++SO42-=BaSO4↓+H2O+CO2↑;
(4)酸铜溶液与氢氧化钾溶液发生复分解反应生成硫酸钾和氢氧化铜沉淀,方程式:Cu2++2OH-═Cu(OH)2↓,
故答案为:Cu2++2OH-═Cu(OH)2↓;
(5)氢氧化钾能够吸空气中的二氧化碳生成碳酸钾和水,部分变质的氢氧化钾含有碳酸钾、氢氧化钾,碳酸钾与硫酸反应生成二氧化碳和水、硫酸钾,离子方程式:CO32-+2H+=H2O+CO2↑氢氧化钾与稀硫酸反应生成硫酸钾和水,离子方程式:H++OH-=H2O;
故答案为:CO32-+2H+=H2O+CO2↑;H++OH-=H2O.
点评 本题考查了电解质的判断,离子方程式的书写,明确电解质的概念及离子方程式书写方法是解题关键,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 大自然利用太阳能最成功的是植物的光合作用 | |
| B. | H2是理想的清洁燃料,储存和运输方便,在现实生活和生产中已大量应用 | |
| C. | 海水淡化技术的进步有助于淡水资源紧缺问题的解决 | |
| D. | 利用工业废气中的CO2制造全降解塑料,符合绿色环保要求 |
| A. | 用重结晶法可除去KNO3晶体中混有少量NaCl晶体 | |
| B. | 实验室制取乙酸丁酯时用水浴加热 | |
| C. | 在硫酸钡悬浊液中加入足量饱和碳酸钠溶液可将其转化为碳酸钡 | |
| D. | 二氧化硫分别通入到硫化钠和硝酸钡溶液中产生沉淀可证明二氧化硫的氧化性和还原性 |
| A. | 比较镁、铝金属性:镁、铝(除氧化膜)分别放入4mol•L-1NaOH溶液中 | |
| B. | 比较氯、溴非金属性:氯气通入溴化钠溶液中 | |
| C. | 比较Cu、Fe2+的还原性:Cu加入FeCl3溶液中 | |
| D. | 比较高锰酸钾、氯气的氧化性:高锰酸钾中加入浓盐酸 |
| A. | 氟氯烃作制冷剂会加剧雾霾天气的形成 | |
| B. | 只通过电解的方法就能实现从食盐水到“84”消毒液的生产 | |
| C. | 加碘食盐中含有碘元素,能使淀粉溶液变蓝 | |
| D. | 工业上制漂白粉,所得的氯化物都具有漂白性 |
| A. | 简单地说,金属的冶炼就是把金属单质从其矿物中分离出来 | |
| B. | 金属冶炼过程中,被冶炼的金属只能被氧化 | |
| C. | 金属冶炼过程中,被冶炼的金属只能被还原 | |
| D. | 金属冶炼过程中,被冶炼的金属既可被氧化,也可被还原 |
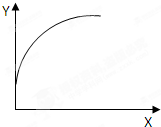 在一密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)=2C(g)+Q(Q>0),当达到平衡后,改变一个条件(X),下列量(Y)一定符合图中曲线的是( )
在一密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)=2C(g)+Q(Q>0),当达到平衡后,改变一个条件(X),下列量(Y)一定符合图中曲线的是( )| X | Y | |
| A | 温度 | 混合气体平均相对分子质量 |
| B | 再加入C | A的质量分数 |
| C | 再加入A | B的转化率 |
| D | 压强 | B的浓度 |
| A. | A | B. | B | C. | C | D. | D |



