题目内容
合成氨对农业生产及国防建设均具有重要意义。
N2(g)+3H2(g)  2NH3(g) △H ="
-92" kJ·mol-1
2NH3(g) △H ="
-92" kJ·mol-1
(1)在恒温恒容密闭容器中进行的合成氨反应,下列能表示达到平衡状态的是_______(填序号)。
a.混合气体的压强不再发生变化
b.混合气体的密度不再发生变化
c.反应容器中N2、NH3的物质的量的比值不再发生变化
d.单位时间内断开a个H-H键的同时形成3 a个N-H键
e.三种物质的浓度比恰好等于化学方程式中各物质的化学计量数之比
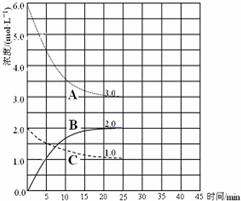
(2)在恒温恒容的密闭容器中,合成氨反应的各物质浓度变化曲线如下图所示。请回答下列问题:

① 表示N2的浓度变化的曲线是 (选填曲线代号“A”、“B”或“C”)。
② 前25 min 内,用H2的浓度变化表示的化学反应平均速率是 。
③在25 min 末反应刚好达到平衡,则该温度下反应的平衡常数K = (计算结果可用分数表示)。
若升高温度,该反应的平衡常数值将_______(填“增大”、“减小”或“不变”)。
(5分)(1) ac (填序号)。(2)①C
② 0.12mol/(L·min) 。
③4/27 减小。
【解析】
试题分析:(1)当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,由此衍生的一些物理性不变,以此解答该题。
b、无论反应是否达到平衡状态,容器内气体的密度都不发生变化,不能判断是否达到平衡状态,故错;d、都为正速率,故错;e、物质的浓度不能判断化学平衡状态,故错。故选ac。
(2)①N2是反应物,结合化学方程式分析,H2的曲线变化快,而N2的变化慢,表示N2的浓度变化的曲线是C。②根据v=△c÷t公式计算得,前25 min 内,用H2的浓度变化表示的化学反应平均速率是0.12mol/(L·min) 。③平衡常数等于生应物的幂之积除以反应物的幂之积,故平衡常数K =4/27。反应为放热反应,升高温度,反应逆向移动,故若升高温度,该反应的平衡常数值将减小。
考点:化学平衡的计算 热化学方程式 电极反应和电池反应方程式 化学平衡的影响因素
点评:本题考查化学平衡计算、平衡常数、热化学方程式、原电池等,综合较大,难度中等,注意两电极反应式相加得总反应式时,两电极得失电子数应相等。

 合成氨对农业生产及国防建设均具有重要意义.已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ?mol-1如图是在恒温恒容密闭容器中进行合成氨反应的图象
合成氨对农业生产及国防建设均具有重要意义.已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ?mol-1如图是在恒温恒容密闭容器中进行合成氨反应的图象下列说法正确的是( )
| A、前25min内,用H2浓度变化表示的化学反应平均速率是0.04 mol?L-1?min-1 | B、在25min 末反应刚好达到平衡,则该温度下反应的平衡常数K=0.148 | C、该反应达到平衡时放出热量为92kJ | D、V正(N2)=2V逆(NH3)说明到达平衡状态 |
 合成氨对农业生产及国防建设均具有重要意义.
合成氨对农业生产及国防建设均具有重要意义. Ⅰ、合成氨对农业生产及国防建设均具有重要意义.
Ⅰ、合成氨对农业生产及国防建设均具有重要意义.
 2NH3(g) △H =" -92" kJ·mol-1
2NH3(g) △H =" -92" kJ·mol-1